Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Основные представлени о методах расчета молекулярных орбиталей. Метод
ХюккеляОрганическая химия / Атомные и молекулярные орбитали / Органическая химия / Атомные и молекулярные орбитали / Основные представлени о методах расчета молекулярных орбиталей. Метод
Хюккеля Основные представлени о методах расчета молекулярных орбиталей. Метод
ХюккеляСтраница 2
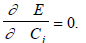
(1.5)
Чтобы получить величины коэффициентов Cj и энергию каждой МО (Ei), операцию (1.5) нужно провести на общей форме приближения ЛКАО МО, которая дается уравнением (1.2). Таким образом, подстановка уравнения (1.2) в уравнения (1.4), если опустить индексы (j) для МО, дает
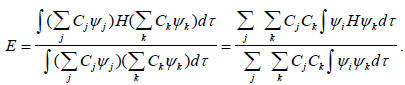
Примем следующие сокращенные обозначения:
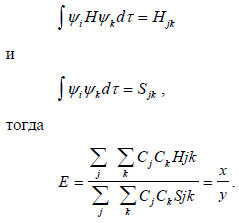
(1.6)
Далее, применяя уравнение (1.5), получаем
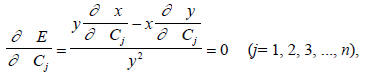
откуда после подстановки уравнения (1.6) имеем
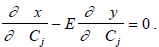
(1.7)
Дифференцируя x и y в уравнении (1.6) по Сj, получим
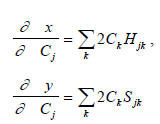
и из уравнения (1.7)
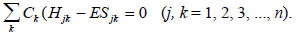
Это и есть вариационное уравнение. Конечным результатом применения вариационного принципа, который позволяет рассчитать коэфициенты С в уравнении (1.2), является система таких уравнений. Для аллильной π-системы, в которой j и k меняются от 1 до 3 и j отстается постоянной в каждом отдельном уравнении, вариационные уравнения имеют вид
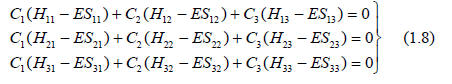
Систему уравнений (1.8) можно решить, составив секулярный детерминант
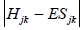
(уравнение 1.9) и решая его для величины Е. Затем значения Е подставляются в уравнения (1.8) и определяются Сij. Интегралы Hjk и Sjk нельзя точно вычислить, так как они получаются слишком сложными. Как раз с этого момента и начинаются расхождения между методом МОХ и более углубленными методами. Вместо попытки решить эти интегралы какими-либо приближенными способами в методе Хюккеля эти интегралы принимают постоянными параметрами, и энергия орбиталей выражается через них. В главе 2 при изложении метода ВМО в качестве меры энергии мы будем использовать постоянные значения кулоновского (α) и резонансного (β) интегралов.
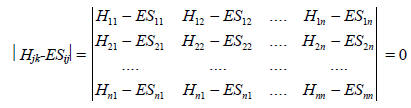
Метод Хюккеля. Основные положения, на которых основан метод МОХ, применяемый для сопряженных π-систем, состоит в следующем:
1) Hjj = α;
2) Hjk = β, если атомы j и k связаны друг и другом,
и Hjk = 0, если атомы j и k не связаны;
3) Sjj = 1; Sjk = 0 для j ≠ k;
4) σ-связи локализованы, и их можно рассматривать как жесткий скелет, окруженный π-электронами.
Интеграл α, называемый кулоновским интегралом, представляет собой энергию электрона на С2р-орбитали. Если рассматривать лишь чисто углеродные системы, то предположение, что для всех атомов Hjj одинаковый, является хорошим приближением; при введении в молекулу π-системы гетероатома α уже не является постоянной величиной. Интеграл β обычно называют резонансным интегралом. Он представляет собой энергию взаимодействия двух атомных орбиталей на соседних атомах j и k. Предположение, что интеграл β всегда одинаков, довольно сомнительно, так как в сопряженных углеводородах степень взаимодействия двух АО может сильно меняться. Например, в бутадиене (рис. 1.23) взаимодействие между первым и вторым атомами углерода будет иным, чем взаимодействие между двумя внутренними атомами, так как длины связей между этими атомами сильно различаются.
Интеграл Sjk называется интегралом перекрывания; для j=k он равен 1. Поскольку для атомных орбиталей
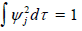
(условие нормировки; разд. 1.3), предположение, что Sjj =1, вполне оправдано. Однако предположение, что Sjk = 0 для j≠k, например, для соседних атомов (k = j +1), совершенно некорректно (по расчетам Робертса, в этом случае Sjk = 0.25).
Четвертое предположение - о том, что σ-связи локализованы, - по-видимому, вполне приемлемо.
Смотрите также
Разложение клетчатки микроорганизмами
Еще в
древности при построении деревянных судов для защиты дерева использовали
асфальт. Во времена Римской империи суда обивали металлическими листами. Выбор
материалов производился экспери ...
Белки молока, строение и функции
В жизни человека наиболее важную роль играет питание.
Оно определяет и физическое состояние, а также физическое и умственное
развитие, повышает иммунитет и т. д.
Молока считается наиболее ...


