Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
МолибденБиблиотека / Библиотека / Молибден МолибденСтраница 1
Электронное строение атома.
4.1. Составьте электронную формулу данного элемента.
Порядковый номер элемента в периодической системе химических элементов Д. И. Менделеева равен 42. Это значит, в молекуле молибдена будет 42 электрона.
Электронная формула молибдена будет такова: ![]()
Составим также его электронно – графическую формулу:
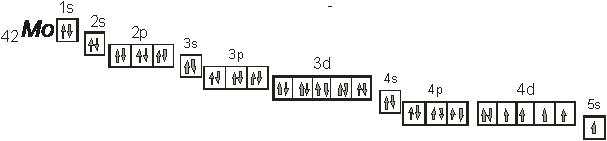
На рисунке выше приведена электронно – графическая формула молибдена.
4.2. Дайте объяснение физического смысла всех индексов у данного химического элемента в системе Д.И. Менделеева (порядковый номер, номер периода, номер группы, принадлежность к группе «А» или «Б»). Определите возможность «Эффекта провала электрона».
Порядковый номер химического элемента в периодической системе химических элементов – 42. у молибдена на электронных уровнях находится 42 электрона, а в ядре должно находится также 42 протона.
Молибден расположен в периодической системе химических элементов в пятом периоде, это значит, что у него будет пять электронных слоев с расположенными на них электронами. Главное квантовое число внешнего электронного уровня равно 5.
Молибден расположен в шестой группе, побочной подгруппе. Молибден относят к элементам подгруппы хрома , в которую входят хром, молибден и вольфрам, которые обладают похожими свойствами. У него будет на электронных уровнях один s-электрон и 5 d-электронов на пред внешнем уровне.
В состав ядра атома изотопа молибдена-96 входят 42 протона (p) и 54 нейтрона (n): ![]() , где массовое число и порядковый номер элемента (число протонов) обозначают числовыми индексами слева от символа химического элемента; верхний индекс означает массовое число, нижний – заряд ядра. Количество нейтронов ядра элементов определяют по массовому числу элемента за вычетом количества протонов.
, где массовое число и порядковый номер элемента (число протонов) обозначают числовыми индексами слева от символа химического элемента; верхний индекс означает массовое число, нижний – заряд ядра. Количество нейтронов ядра элементов определяют по массовому числу элемента за вычетом количества протонов.
Таким образом, в состав атома молибдена входят ядро, состоящее из 42 протонов, 54 нейтронов и электронное облако, представленное 42 электронами.
Вследствие устойчивости d5-конфигурации энергетически оказывается более выгодным переход одного из ns-электронов в (n-1) d-состояние. Поэтому молибден, как и хром в s-состоянии внешнего уровня имеют по одному, а в предпоследнем слое по 13 электронов. Таким образом, имеет место «проскок» электрона:
![]()
Проскок электрона можно объяснить с точки зрения квантово-механических представлений повышенной энергетической стабильностью конфигурации: 4d5.
4.3. Выделите валентные подуровни в электронной формуле атома химического элемента, определите принадлежность химического элемента к типу s-, p-, d-, f-элементов.
Покажем расположение валентных электронов в атоме молибдена. Как видно из электронной формулы моилбден относится к d-элементам, поскольку у него заполняется 4d-подуровень.
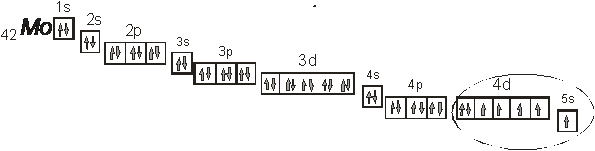
![]()
На приведенном рисунке эллипсом выделено расположение валентных электронов в атоме молибдена. Как видно в создании химической связи будут брать участие электроны как 5s- так и 4d-подуровня.
4.4. Напишите наборы квантовых чисел для всех валентных электронов.
У атома молибдена будет разное количество валентных электронов приразных степе5нях окисления, до шести включительно. Запишем наборы квантовых чисел для этих электронов.
Сначала рассмотрим электроны на 5s-подуровне. Главное квантовое число равно 5 и химический элемент находится в 5 периоде периодической системы химических элементов. Поскольку в молибдена валентный электрон расположен на s-подуровне то его орбитальное квантовое число имеет значение равное 0. Поскольку электрон будет только один, то его спин будет иметь значение ms
= +1/2. Поскольку ml
= 0 то у элемента не будет других подуровней кроме s-подуровня.
Набор квантовых чисел будут иметь вид:
n
= 5; l
= 0; ml
= 0; ms
= +1/2.
Рассмотрим электроны на 4d-подуровне. Их количество равно 5. главное квантовое число п равно 4, ![]() . Орбитальное квантовое число равно
. Орбитальное квантовое число равно ![]() и орбитальное квантовое число может принимать значения равные 0, 1, 2, 3. магнитное квантовое число может принимать значения в пределах от +l до -l. Поскольку
и орбитальное квантовое число может принимать значения равные 0, 1, 2, 3. магнитное квантовое число может принимать значения в пределах от +l до -l. Поскольку ![]() то ml
то ml
Смотрите также
Эпитаксиальный рост Ge на поверхности Si(100)
С физикой
тонких пленок связаны достижения и перспективы дальнейшего развития
микроэлектроники, оптики, приборостроения и других отраслей новой техники.
Успехи микроминиатюризации электронн ...
Гидроксикарбонильные соединения. Дикарбоновые кислоты
a-Гидроксикарбонильные
соединения, как уже отмечалось, могут быть получены окислением диолов
гипобромитом натрия или реагентом Фентона.
Для
a-гидроксикарбонильных
соединений характерна ...
Экспериментальные
результаты и обсуждения
Зависимости
поверхностного давления от площади, приходящейся на одну молекулу (p-A изотермы) для
гомо - и гетеромолекулярных плавающих слоев на основе С60, ДБ24К8 и магнитного
комплекс пр ...


