Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
МолибденБиблиотека / Библиотека / Молибден МолибденСтраница 2
= -2, -1, 0, +1, +2. Согласно правила Хунда суммарный спин должен быть максимальным, поэтому мы можем считать, что спин электронов будет равен +1/2.
Запишем наборы квантовых чисел для электронов.
n
= 5; l= 2; ml
= -2 ; ms
= +1/2.
n
= 5; l= 2; ml
= -1 ; ms
= +1/2.
n
= 5; l= 2; ml
= 0 ; ms
= +1/2.
n
= 5; l= 2; ml
= +1 ; ms
= +1/2.
n
= 5; l
= 2; ml
= +2 ; ms
= +1/2.
4.5. Определите принадлежность химического элемента к металлам или неметаллам, спрогнозируйте величины степени окисления.
Поскольку молибден расположен в шестой группе периодической системы, и не в главной подгруппе, а в побочной, то он относится к металлам. В химических реакциях он будет проявлять металлические свойства. Для металлов более приемлема отдача электронов. Поэтому молибден может отдавать максимум шесть электронов с ![]() - подуровня и с 4d-подуровня. Поэтому молибден будет проявлять степень окисления +2, +3, +4, +5, +6. соединения с этими степенями окисления обладают разной стойкостью, наиболее стойкими будут соединения с степенью окисления равной +6.
- подуровня и с 4d-подуровня. Поэтому молибден будет проявлять степень окисления +2, +3, +4, +5, +6. соединения с этими степенями окисления обладают разной стойкостью, наиболее стойкими будут соединения с степенью окисления равной +6.
4.6. Распределите валентные электроны атома химического элемента по энергетическим ячейкам в соответствии с принципом наименьшей энергии и правилом Гунда.
В соответствии с принципом наименьшей энергии валентный электрон атома молибдена расположен на 5s-подуровне, поскольку он располагает меньшей энергией чем любой другой подуровень. Правило Хунда гласит, что устойчивому состоянию атома отвечает такое расположение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. Поэтому электроны на 4d-подуровне расположатся таким образом как на приведенном рисунке:
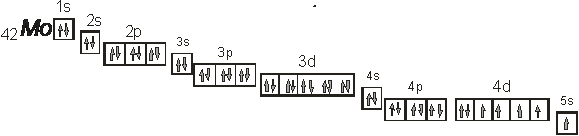
4.7. Прогнозируйте тип гибридизация валентных атомных орбиталей при образовании бинарных соединений (фторидов, хлоридов и др.).
Рассмотрим получение ![]() :
:
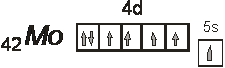
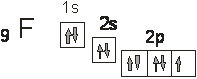
![]()
Ион молибдена (VI) имеет на 4d-уровне 0 электронов, а также свободные 4s и 4p-орбитали. Образование связи можно рассматривать как донорно-акцепторный процесс (ион молибдена – акцептор, гидрид-, фторид- и хлорид-ионы – доноры). В бинарных соединениях образуется 6 связей Мо-Э, для каждой из них атом молибдена предоставляет одну свободную орбиталь. Тип гибридизации sd5 (форма октаэдрическая). Следует отметить, что для молибдена характерны разные соединения с галогеними, поэтому и гибридизация в этих соединениях будет разной. Например в трифториде MоF3 для создания химической святи использовано только три электрона: sd2 (форма тетраэдрическая).
Соединение данного химического элемента с неметаллами.
Рассмотрим реакции взаимодействия молибдена с неметаллами. Молибден довольно активно реагирует с неметаллами (кремнием, бором, галогенами, серой и т. п.), учитывая то что молибден имеет несколько степеней окисления то получается в таких реакциях несколько продуктов.
5.1. С водородом.
Молибден не реагирует с водородом с получением химических соединений. Имеет место только физическое растворение водорода в молибдене с образованием нестойких связей. Растворимость водорода в молибдене растет с повышением температуры до 0,5 см3 в 100 граммах металла.
5.2. С галогенами.
С молибденом фтор образует летучие фториды. Хлор и бром ре6агируют с ним при температуре красного каления. Йод реагирует с молибденом очень медленно. В присутствии влаги реакция с галогенами ускоряется и она становится возможной даже на холоду.
Молибден образует гексафторид MoF6, пентафторид MoF5, тетрафторид MOF4 и трифторид MоF3; гексахлорид МоС16, пентахлорид МоС15, тетрахлорид МоС13, трихлорид МоС13 и комплексный псевдодихлорид [Мо6(С1)8]С14; тетрабромид МоВг4, трибромид МоВг3 и комплексный псевдодибромид [Мо6Вг8]Вг4. С иодом достоверно известно лишь два соединения – дииодид МоІ2 и трииодид МоІ3. Помимо этих соединений, известен ряд оксигалогенидов и несколько менее достоверных соединений.
Фториды.
Гексафторид получается действием сухого фтора в смеси с азотом на металл (в платиновой трубке), трифторида брома на металл при 250°, безводного HF на MoCl5:
Смотрите также
Ультрафиолетовое отверждение лаков и красок
На сегодняшний
момент в различных областях науки и промышленности ведутся активные
исследования, направленные на создание ресурсо- и энергосберегающих
экологически безопасных технологий. В ...
Одноосновные насыщенные карбоновые кислоты
...
Приложение
Рис.1. Спектры
оптического поглощения образцов синей и прозрачной соли из Соликамска и Польши.
Рис.2. Декомпозиция спектров оптического
поглощения ка ...


