Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Процессы, механизмы и кинетические модели в синтетической химииУчим химию / Учим химию / Процессы, механизмы и кинетические модели в синтетической химии Процессы, механизмы и кинетические модели в синтетической химииСтраница 4
где a – объемный коэффициент теплоотдачи (кал/(л·час·гр)), Q – количество выделяемого тепла (кал/моль), Cfb – скорость реакции в диффузионном режиме, b – коэффициент скорости диффузии, Cf – концентрация спирта в потоке.
При равенстве qподв = qотв,
![]() ,
,
где n – теплоемкость, кал/(л·гр).
Режим зажигания устанавливается при
![]() , где
, где ![]() ,
,
Е – наблюдаемая энергия активации процесса.
В режиме диффузионного "зажигания" Tf = 650 – 700оС, Тз = 900 – 1000оС, но при малых временах контакта селективность процесса достигает 95% при 90% конверсии метанола. Полученный в результате абсорбции водой раствор 40% формальдегида (формалин) можно использовать как товарный продукт.
Окислительное хлорирование этилена до дихлорэтана. Процесс синтеза дихлорэтана (ДХЭ) по реакции
![]()
протекает в области 325 – 525оС (лучше 350 – 400оС) на меднохлоридных катализаторах CuCl-KCl/SiO2 или CuCl2/g-Al2O3 практически при 100% конверсии HCl с выходом ДХЭ по этилену ~ 96%. Дихлорэтан образуется на поверхности катализатора без участия свободного Cl2. Механизм реакции изучен весьма детально. Схема механизма приведена ниже для второго катализатора.
![]()
![]()
![]()
![]()
![]()
![]()
Если вектор стехиометрических чисел стадий маршрута равен |2 2 2 2 1 1|, получим итоговое уравнение. Скорость образования ДХЭ описывается уравнением с учетом 2-х медленных стадий (3) и (5):
![]() ,
,
где 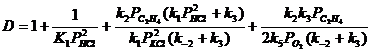 .
.
При PHCl ³ 2 кПа реализуется нулевой порядок по PHCl, и при определенных соотношениях констант уравнение преобразуется к виду
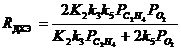
Реакции окисления в промышленной неорганической химии
Каталитические процессы активно применяются для окисления неорганических соединений с целью получения полезных продуктов и для очистки газовых выбросов и водных стоков.
![]()
(процессы дожигания СО, очистка воздуха помещений)
![]()
(получение серы, очистка природного и попутных газов от H2S)
![]()
(процесс Клауса, очистка газовых выбросов и синтез серы)
![]()
(производство H2SO4)
Смотрите также
Фазовые равновесия в системе MgS-Y2S3
Соединения с участием
РЗЭ остаются по прежнему обширным резервом для создания новых материалов.
Возможно создание материалов с уникальными, заранее заданными свойствами.
Взаимодействие в
...
Амилолитические ферменты и их применение в спиртовой промышленности
...


