Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Концентрация растворовОткрытая химия / Растворы / Открытая химия / Растворы / Концентрация растворов Концентрация растворовСтраница 1
Важной характеристикой растворов служит их концентрация, которая выражает относительное количество компонентов в растворе. Различают массовые и объемные концентрации, размерные и безразмерные.
К безразмерным концентрациям (долям) относятся следующие концентрации: l Массовая доля растворенного вещества W (B) выражается в долях единицы или в процентах:
| |
где m (B) и m (A) – масса растворенного вещества B и масса растворителя A. l Объемная доля растворенного вещества σ (B) выражается в долях единицы или объемных процентах:
 |
где Vi – объем компонента раствора, V (B) – объем растворенного вещества B. Объемные проценты называют градусами*). *) Иногда объемная концентрация выражается в тысячных долях (промилле, ‰) или в миллионных долях (млн–1), ppm. l Мольная доля растворенного вещества χ (B) выражается соотношением
| |
Сумма мольных долей k компонентов раствора χi равна единице ![]()
К размерным концентрациям относятся следующие концентрации: l Моляльность растворенного вещества Cm (B) определяется количеством вещества n (B) в 1 кг (1000 г) растворителя, размерность моль/кг.
| |
l Молярная концентрация вещества B в растворе C (B) – содержание количества растворенного вещества B в единице объема раствора, моль/м3, или чаще моль/литр:
| |
где μ (B) – молярная масса B, V – объем раствора. l Молярная концентрация эквивалентов вещества B CЭ (B) (нормальность – устаревш.) определяется числом эквивалентов растворенного вещества в единице объема раствора, моль∙литр–1:
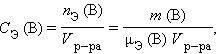 |
Смотрите также
Определение свойств газов
Общие сведения о свойствах
газов
В природе в
нормальных условиях (при комнатной температуре и атмосферном давлении)
сравнительно немногие химические вещества находятся в газообразном сос ...
Галогены
Галогены
(от греч. halos – соль и genes – рождающий, рождённый) находятся в главной
подгруппе VII группы периодической системы химических элементов.
К
галогенам относят фтор, хлор, бром, ...
Заключение
В процессе
проделанной работы была рассчитана ректификационная колонна для разделения
смеси бензол–толуол.
В
результате расчета получены данные:
1) &nbs ...


