Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Распространенные элементы. строение атомов. Электронные
оболочки. ОрбиталиCправочник по химии для подготовки к ЕГЭ / Cправочник по химии для подготовки к ЕГЭ / Распространенные элементы. строение атомов. Электронные
оболочки. Орбитали Распространенные элементы. строение атомов. Электронные
оболочки. Орбитали
Химический элемент– определенный вид атомов, обозначаемый названием и символом и характеризуемый порядковым номером и относительной атомной массой.
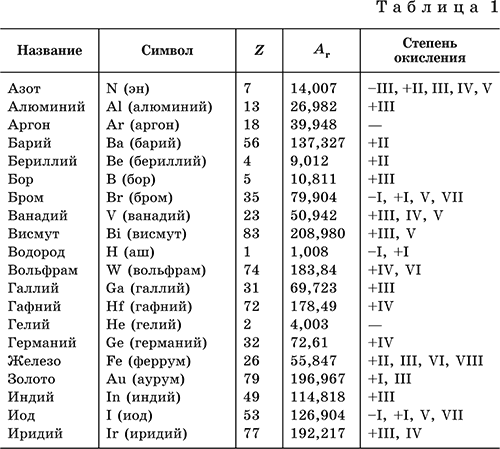
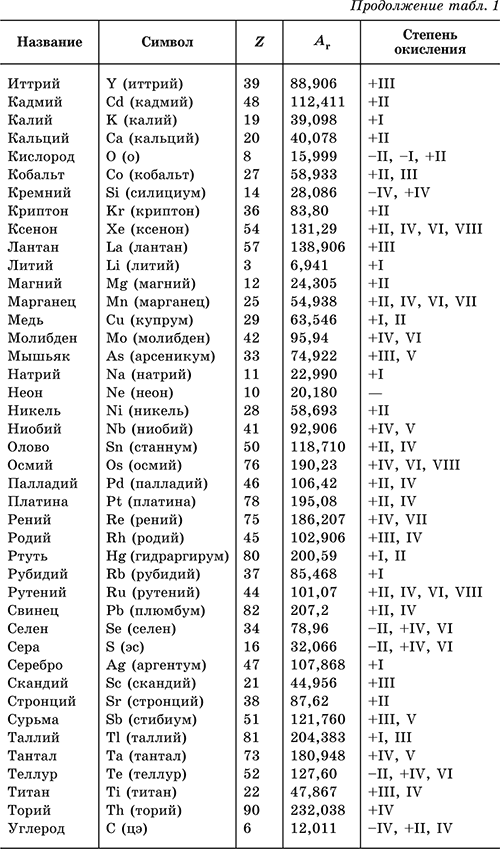
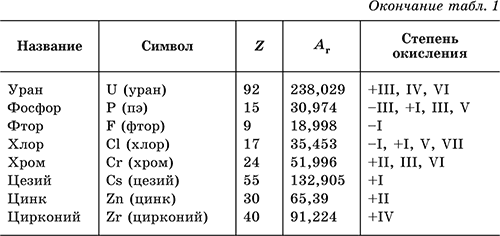
В табл. 1 перечислены распространенные химические элементы, приведены символы, которыми они обозначаются (в скобках – произношение), порядковые номера, относительные атомные массы, характерные степени окисления.
Нулевая
степень окисления элемента в его простом веществе (веществах) в таблице не указана.
Все атомы одного элемента имеют одно и то же число протонов в ядре и число электронов в оболочке. Так, в атоме элемента водород Н находится 1р+ в ядре и на периферии 1е‑; в атоме элемента кислород О находится 8р+ в ядре и 8е‑ в оболочке; атом элемента алюминий Аl содержит 13р+ в ядре и 13е‑ в оболочке.
Атомы одного элемента могут различаться числом нейтронов в ядре, такие атомы называются изотопами. Так, у элемента водород Н три изотопа: водород‑1 (специальное название и символ протий 1H) с 1 р+ в ядре и 1е‑ в оболочке; водород‑2 (дейтерий 2Н, или D) с 1р+ и 1п0 в ядре и 1е‑ в оболочке; водород‑3 (тритий 3Н, или Т) с 1р+ и 2п0 в ядре и 1е‑ в оболочке. В символах 1Н, 2Н и 3Н верхний индекс указывает массовое число– сумму чисел протонов и нейтронов в ядре. Другие примеры:
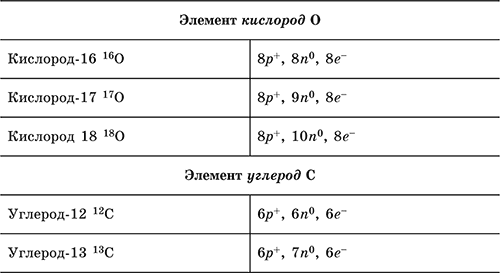
Электронную формулу атома любого химического элемента в соответствии с его расположением в Периодической системе элементов Д. И. Менделеева можно определить по табл. 2.

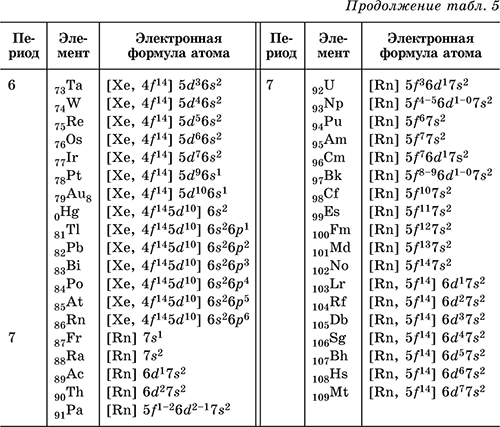
Электронная оболочка любого атома делится на энергетические уровни (1, 2, 3‑й и т. д.), уровни делятся на подуровни (обозначаются буквами s, р, d, f). Подуровни состоят из атомных орбиталей – областей пространства, где вероятно пребывание электронов. Орбитали обозначаются как 1s (орбиталь 1‑го уровня s‑подуровня), 2s, 2р, 3s, 3р, 3d, 4s… Число орбиталей в подуровнях:

Заполнение атомных орбиталей электронами происходит в соответствии с тремя условиями:
1) принцип минимума энергии
Электроны заполняют орбитали, начиная с подуровня с меньшей энергией.
Последовательность нарастания энергии подуровней:
1s < 2c < 2p < 3s < 3p < 4s ≤ 3d < 4p < 5s ≤ 4d < 5p < 6s…
2) правило запрета (принцип Паули)
В каждой орбитали может разместиться не более двух электронов.
Один электрон на орбитали называется неспаренным, два электрона – электронной парой:

3) принцип максимальной мультиплетности (правило Хунда)
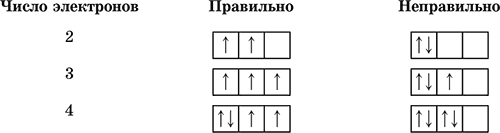
В пределах подуровня электроны сначала заполняют все орбитали наполовину, а затем – полностью.
Каждый электрон имеет свою собственную характеристику – спин (условно изображается стрелкой вверх или вниз). Спины электронов складываются как вектора, сумма спинов данного числа электронов на подуровне должна быть максимальной
(мультиплетность):
Заполнение электронами уровней, подуровней и орбиталей атомов элементов от Н (Z = 1) до Kr (Z = 36) показано на энергетической диаграмме (номера отвечают последовательности заполнения и совпадают с порядковыми номерами элементов):
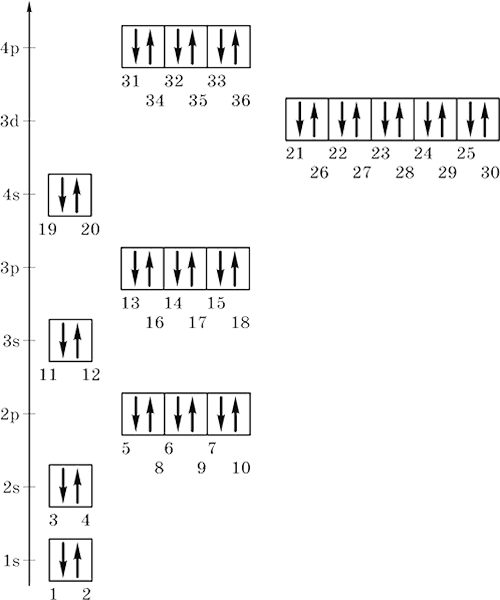
Из заполненных энергетических диаграмм выводятся электронные формулы атомов элементов. Число электронов на орбиталях данного подуровня указывается в верхнем индексе справа от буквы (например, 3d5 – это 5 электронов на Зd‑подуровне); вначале идут электроны 1‑го уровня, затем 2‑го, 3‑го и т. д. Формулы могут быть полными и краткими, последние содержат в скобках символ соответствующего благородного газа, чем передается его формула, и, сверх того, начиная с Zn, заполненный внутренний d‑подуровень. Примеры:
1H = 1s1
2Не = 1s2
3Li = 1s22s1 = [2He]2s1
8O = 1s22s22p4
= [2He]2s22p4
13Al = 1s22s22p63s23p1
= [10Ne]3s23p1
17Cl = 1s22s22p63s23p5
= [10Ne]3s23p5
2OСа = 1s22s22p63s23p4s2
= [18Ar]4s2
21Sc = 1s22s22p63s23p63d14s2
= [18Ar]3d14s2
25Mn = 1s22s22p63s23p63d54s2
= [18Ar]3d54s2
26Fe = 1s22s22p63s23p63d64s2
= [18Ar]3d64s2
3OZn = 1s22s22p63s23p63d104s2
= [18Ar, 3d10]4s2
33As = 1s22s22p63s23p63d104s24p3
= [18Ar, 3d10]4s24p3
36Kr = 1s22s22p63s23p63d104s24p6
= [18Ar, 3d10]4s24p6
Электроны, вынесенные за скобки, называются валентными. Именно они принимают участие в образовании химических связей.
Исключение составляют:
24Cr = 1s22s22p63s23p63d54s1
= [18Аr]Зd54s1
(а не 3d44s2!),
29Cu = 1s22s22p63s23p63d104s1
= [18Ar]3d104s1
(а не 3d94s2!).
Примеры заданий части А
1. Название, не относящееся
к изотопам водорода, – это
1) дейтерий
2) оксоний
3) протий
4) тритий
2. Формула валентных подуровней атома металла – это
1) 4s24p4
2) 3d54s2
3) 2s22p1
4) 3s23p6
3. Число неспаренных электронов в основном состоянии атома железа равно
1) 2
2) 3
3) 4
4) 8
4. В возбужденном состоянии атома алюминия число неспаренных электронов равно
1) 1
2) 2
3) 3
4) 4
5. Электронная формула [Ar]3d94s0 отвечает катиону
1) Ti2+
2) Cu2+
3) Cr2+
4) Zn2+
6. Электронная формула аниона Э2‑ [Ne] 3s23p6 отвечает элементу
1) аргон
2) хлор
3) сера
4) фосфор
7. Суммарное число электронов в катионе Mg2+ и анионе F‑ равно
1) 9
2) 10
3) 20
4) 21


