Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Кинетическая модель и механизм
полимеризацииУчим химию / Обзор и математическое моделирование суспензионной полимеризации тетрафторэтилена / Учим химию / Обзор и математическое моделирование суспензионной полимеризации тетрафторэтилена / Кинетическая модель и механизм
полимеризации Кинетическая модель и механизм
полимеризацииСтраница 1
Изучение кинетики и механизма суспензионной полимеризации тетрафторэтилена в воде представляет собой очень сложную задачу. Независимо от условий полимеризации уже на начальной стадии роста макрорадикала образуется твердая фаза полимера, и на протяжении всего процесса полимеризация носит ярко выраженный гетерогенный характер.
Инициирование полимеризации осуществляется в водном растворе, где в результате взаимодействия радикалов инициатора с растворенным тетрафторэтиленом начинается рост молекулы полимера. Далее происходит агрегация молекул с образованием нерастворимых частиц полимера, которые в дальнейшем и становятся центрами полимеризации. Образующиеся частицы имеют рыхлую структуру и из-за несмачиваемости политетрафторэтилена водой всплывают на поверхность. Их поры заполнены мономером, и полимеризация в дальнейшем протекает непосредственно в газовой фазе с резко возрастающей скоростью. Первая гомогенная стадия полимеризации непродолжительная и длится секунды или доли секунды.
При использовании в качестве инициатора персульфата аммония механизм этой реакции можно представить в виде следующих стадий:
1) Образование из исходного персульфата радикалов, инициирующих полимеризацию:
2)
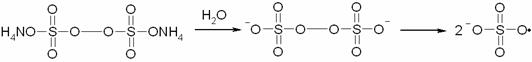
![]()
3) Инициирование:
![]()
4) Рост цепи:
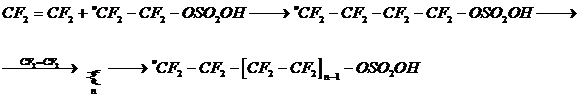
5) Обрыв цепи, который возможен по двум направлениям:
а) Столкновение растущего макрорадикала с радикалом инициатора:
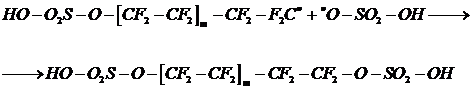
б) Рекомбинация двух макрорадикалов:
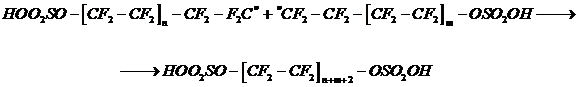
Высокая прочность связи ![]() в политетрафторэтилене (около 460,5 кДж/моль) и еще более высокая прочность этой связи в тетрафторэтилене (485,7 кДж/моль), а также высокая чистота применяемых при полимеризации мономера и среды, позволяют почти полностью исключить как передачу цепи, так и обрыв цепи за счет диспропорционирования.
в политетрафторэтилене (около 460,5 кДж/моль) и еще более высокая прочность этой связи в тетрафторэтилене (485,7 кДж/моль), а также высокая чистота применяемых при полимеризации мономера и среды, позволяют почти полностью исключить как передачу цепи, так и обрыв цепи за счет диспропорционирования.
В связи с нерастворимостью ПТФЭ и растущих макрорадикалов в воде, обрыв цепи в результате рекомбинации радикалов также мало вероятен, но, в принципе, возможен.
Таким образом, при минимальном количестве инициатора можно получать полимер с рекордно большой молекулярной массой (107 и более).
Скорость полимеризации убывает в следующем ряду фторолефинов:
CF2=CF2 >
CF2=CHF >
CF2=CH2 >
CFH=CH2 >
CF2=CFC1 >
СF3СF=СF2
Очень высокую скорость полимеризации ТФЭ объясняют сильным уменьшением электронной плотности π-связи вследствие наличия в ТФЭ четырех расположенных симметрично отрицательных атомов фтора.
Наиболее детально изучена кинетика полимеризации ТФЭ в воде при давлении ниже атмосферного. Определены константы элементарных актов роста и обрыва цепи, а также выведено уравнение для общей скорости полимеризации под действием персульфата аммония при 40—70 °С и давлении до 101 кПа (760 мм рт. ст.).
Зависимость скорости от продолжительности полимеризации характеризуется небольшим нестационарным участком, после чего она остается постоянной до значительной степени превращения мономера. На стационарном участке во всем изученном интервале температур сохраняется линейная зависимость скорости от концентрации ТФЭ. Зависимость скорости полимеризации от концентрации инициатора носит сложный характер (рис. 1). При невысокой концентрации инициатора (до максимума на кривых) наблюдается линейная зависимость v от Син. Для этих концентраций инициатора получены выражения для общей скорости полимеризации и констант роста и обрыва цепи, в л/(моль·с):
Смотрите также
Жизнь и деятельность Д.И. Менделеева
...
Полимераналогичные превращения бутадиен-стирольных каучуков
Под реакциями полимеров понимают все химические превращения
заранее образовавшихся макромолекул. Эти реакции могут протекать с сохранением,
увеличением или уменьшением степени полимеризации. ...


