Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Общая методика синтеза a-замещённых нитронов.Библиотека / Реакции a-литиированных циклических нитронов с электрофильными реагентами / Библиотека / Реакции a-литиированных циклических нитронов с электрофильными реагентами / Общая методика синтеза a-замещённых нитронов. Общая методика синтеза a-замещённых нитронов.Страница 2
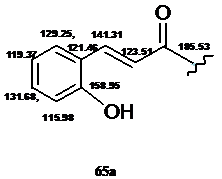
1-(3,3-Диметил-2-гидрокси-3,4-дигидроизохинолин-1-ил)-3-(2-гидроксифенил)-пропенон 65б.
ЯМР 1Н (DMSO-d6,d, м.д.): 1.39 (c, 6H, CH3), 3.22 (c, 2H, CH2), 6.8-7.0 (м, 3H, аром.), 7.2-7.4 (м, 4H, аром.), 7.6-7.7 (м, 1Н, аром.), 7.74 (AB, 1Н, СН=СН, 3JHH = 16 Гц), 7.05 (AB, 1Н, СН=СН, 3JHH = 16 Гц), 10.3 (с, ушир, 1Н). Спектр ЯМР 13C (DMSO-d6,d, м.д.): 23.73 (2 СН3), 66.93, 116.21, 119.37, 120.54, 124.43, 126.74, 127.24, 128.06, 128.66, 128.69, 130.10, 132.52 (аром.), 157.12 (C
-OH), 122.91 (C
=C-Ar), 141.01 (C=C
-Ar), 138.00 (С=N), 190.86 (С=О).

3-(2-Метоксифенил)-1-(1,2,2,5,5-пентаметил-3-имидазолин-3-оксид-4-ил)-пропенон 67
. ЯМР 1Н (СDCl3, d, м.д.): 1.44 (c, 3H, CH3), 1.50 (c, 3H, CH3), 2.36 (c, 3H, NCH3), 3.86 (c, 3H, ОCH3), 6.6 –7,0 (м, 2H, аром.), 7.3 – 7,4 (м, 1Н, аром.), 7.6 – 7,7 (м, 1Н, аром.), 8.18 (с, 2Н, СН
=СН
). ЯМР 13C (DMSO-d6, d, м.д.): 23.61, 24.27 (СH3), 26.51 (NСH3), 55.48 (OСH3), 64.17 (C2), 92.59 (С5), 111.06, 120,59, 128.67, 131.60 (аром.), 124.06 (ипсо-аром.), 124.64 (С
=С-Ar), 139.60 (С=С
-Ar), 143.20 (С=N), 156.60 (MeO-С-аром.), 182.40 (С=О).
Масс-спектр: найдено M+=316,17868, вычислено для C18H24N2O3. М+= 316,17869.
2-Диметиламинометил-(1,2,2,5,5-пентаметил-3-имидазолин-3-оксид-4-ил)-1-гидрокси-l-фенил-пропен-2 69.
Остаток, полученный после упаривания органического экстракта хроматографировали на препаративной пластине с Al2O2, элюент – EtOAc- гексан (2:3). ЯМР 1Н (СDCl3, d, м.д.): 1.01, 1.43, 1.46, 1.49 (с, 4СН3), 2.21 (с, 6Н, N-(CH
3)2), 2.29 (с, 3Н, N-CH
3), 2.96 (AB, 1Н, H-C-H
,2J = 12 Гц), 3.22 (AB, 1Н, H
-C-H ,2J = 12 Гц), 4.55(с, 1H, С=СНН
), 5.00 (с, 1H,С=СН
Н), 7.2-7.4 (м, 3Н, аром.), 7.5-7.6 (м, 2Н, аром.), 7.74-8.04 (с, ушир., 1Н, О-Н
). ЯМР 13C (СDCl3:С6D6 - 1:1, d, м.д.): 17.21, 18.91 м.д., 19.10 (6 CH3), 20.60 (N-CH3), 38.80 (N(C
H3)2), 60.00 (С2), 60.20 (С
Н2N), 75.00 (С5), 83.80 (PhC
HOH), 111.53 (C=C
H2), 126.48, 126.90, 127.86 (аром.), 137.54 (ипсо-аром.), 140.47 (C
=CH2), 144.17 (С=N).
2-Диметиламинометил-(3,3,5,5-тетраметилпирролин-1-оксид-4-ил)-1-гидрокси-l-фенилпропен-2 69а.
Остаток, полученный после упаривания органического экстракта хроматографировали на препаративной пластине с Al2O2, элюент – EtOAc- гексан (1:3). ЯМР 1Н (СDCl3, d, м.д.): 0.96, 1.38, 1.46, 1.47 (с, 4СН
3), 1.81 (AB, 1Н, H
-C-H ,2J = 12.9 Гц), 1.91 (AB, 1Н, H-C-H, 2J = 12.9 Гц), 2.25 (с, 6Н, N-(CH
3)2), 2.91 (AB, 1Н, H
-C-H ,2J = 12.8 Гц), 3.19 (AB, 1Н, H-C-H,2J = 12.8 Гц), 4.49 (с, 1Н, С=СНН
), 4.99 (с, 1Н, С=СН
Н), 7.2-7.4 (м, 3Н, аром.), 7.5-7.6 (м, 2Н, аром.), 7.7-8.0 (с, ушир, 1Н, О-Н
). ЯМР 13C (СDCl3,d, м.д.): 26.75, 28.02, 28.74, 30.52 (6 CH3), 42.79 (С3), 44.67 (N(C
H3)2), 50.22 (С4), 65.60 (С
Н2N(CH3)2), 72.01 (С5), 81.28 (PhC
HOH), 116.60 (C=C
H2), 126.48, 127.07, 127.52 (аром.), 142.98 (C
=CH2), 146.05 (ипсо-аром.), 153.59 (С=N).
1,2,2,5,5-Пентаметил-4-бензоил-3-имидазолин-3-оксид 71.
После упаривания органического экстракта получили маслообразный продукт, который хроматографировали на препаративной пластине с селикагелем, элюент – хлороформ – метанол (3 %). ЯМР 1Н (СDCl3, d, м.д.): 1.43 (c, 3H, CH3), 1.53 (c, 3H, CH3), 2.41 (c, 3H, CH3), 7.2-7.9 (м, 5Н, аром.). ЯМР 13C (СDCl3, d, м.д.): 24.22 (4 C
H3), 26.91 (N-C
H3), 64.33 (С5), 91.84 (C2), 128.62, 128.87 (аром.), 133.65 (п-аром.), 136.16 (ипсо-аром.), 144.21 (С=N).
Смотрите также
Процессы адгезии и когезии
...
Увеличение степени защиты стали от коррозии в нейтральных и кислых средах
Работа посвящена
проблеме увеличения степени защиты стали от коррозии в нейтральных и кислых
средах, при использовании фосфорсодержащих ингибиторов, а также
совершенствованию дискретных мет ...
Физико-химические методы определения фенола
Аналитическая химия – наука о методах определения химического состава
вещества и его структуры. Однако это определение КС представляется
исчерпывающим. Предметом аналитической химии являются ...


