Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Механизмы гомогенного катализа.Статьи и работы по химии / Гомогенный катализ / Статьи и работы по химии / Гомогенный катализ / Механизмы гомогенного катализа. Механизмы гомогенного катализа.Страница 1
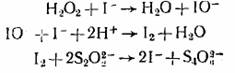 |
Эта схема представляет собой циклический маршрут с итоговым уравнением
в двух первых стадиях которого катализатор расходуется, а в последней снова регенерируется.
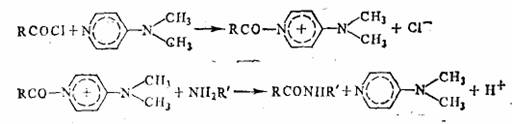
В качестве второго примера можно привести реакцию хлорангидридов карбоновых
 |
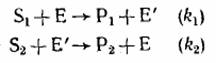 |
Такой механизм катализа часто встречается в окислительно-восстановительных реакциях, и роль катализатора в этом случае сводится к созданию нового, более эффективного пути переноса электрона от восстановителя к окислителю.
 |
Второй, наиболее распространенный механизм действия катализаторов включает в качестве первой стадии обратимое взаимодействие одного или нескольких субстратов с катализатором с образованием комплекса катализатор — субстрат. Так протекает катализ химических превращений ионами металлов и их координационными соединениями и катализ ферментами. К этому же типу можно отнести катализ кислотами, поскольку он включает, как правило, присоединение протона к одному из субстратов, что можно рассматривать как образование комплекса протон—субстрат.
Комплексообразование может приводить к нескольким различным эффектам, обеспечивающим ускорение реакции.
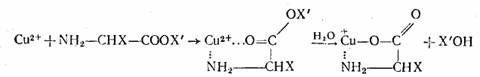 |
Смотрите также
Фенолы. Реакции нуклеофильного замещения ароматических соединений. Получение фенолов
...
Анализ биологических тканей и жидкостей
Химия всегда была
связана с медициной, а в XVI-XVII в.в. практически целиком
«работала» на нее (период ятрохимии). Многие химики тех времен были по
образованию, а иногда и по роду занятий, ...
Создание новых лекарственных веществ
Несмотря на достижения
современной анестезии, продолжаются поиски менее опасных средств для наркоза,
разработка различных вариантов многокомпонентного избирательного наркоза,
позволяющего з ...


