Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Механизмы гомогенного катализа.Статьи и работы по химии / Гомогенный катализ / Статьи и работы по химии / Гомогенный катализ / Механизмы гомогенного катализа. Механизмы гомогенного катализа.Страница 2
Поскольку ион металла при образовании координационной связи выступает как электрофильный компонент, этот тип катализа получил название электрофильного катализа.
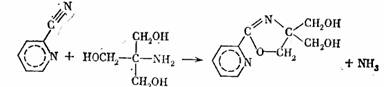 |
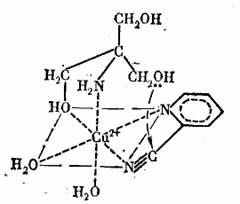
Основными факторами при этом являются поляризация связи С=N в нитриле, облегчающая нуклеофильную атаку на атом (в результате этого ионы Сu+ являются катализаторами щелочного гидролиза нитрила), и одновременная координация обоих субстратов, обеспечивающая в лимитирующей стадии процесса атаку ОН-группы триса на поляризованный атом С нитрила (замыкание цикла с отщеплением аммиака происходит, по-видимому, в последующих стадиях, возможно, уже вне комплекса; стрелкой показано направление атаки атома О триса на атом С нитрила).
 |
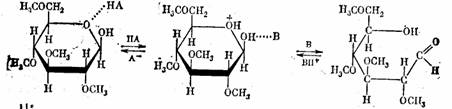 |
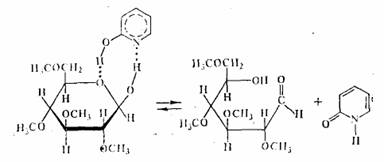
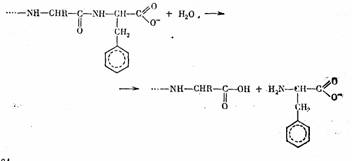
Реакция катализируется эквимолярной смесью фенола (кислота НА) и пиридина (основание В). Учитывая, что образовавшийся в комплексе катион пиридиния (ВH+) должен передать протон фенолят-иону (А-), легко видеть, что в этой реакции разрываются четыре связи и образуются четыре новые связи.
 |
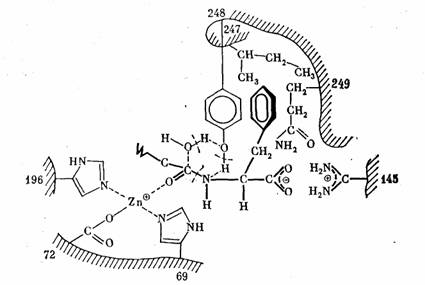
Наиболее полно и совершенно все перечисленные факторы, обеспечивающие воздействие катализатора на субстраты, используются в биологических катализаторах — ферментах. В настоящее время в результате успешного развития рентгеноструктурного анализа белков установлена полная пространственная структура ряда ферментов и их комплексов с субстратами. В качестве примера на рис. 1 приведена схема взаимодействия фермента карбоксипептидазы с субстратом.
 |
На рис. 1 изображен концевой фрагмент расщепляемой полипептидной цепи и функциональные группы фермента, принимающие то или иное участие в каталитическом процессе. Два имидазольных кольца (остатки аминокислоты гистидина) и карбоксильная группа остатка глутаминовой кислоты координированы с ионом цинка, заряд которого тем самым наполовину нейтрализован. Протонированная гуанидиновая группа (остаток аминокислоты аргинина) взаимодействует с ионизованной концевой карбоксильной группой субстрата. Этот же концевой аминокислотный остаток связан своим ароматическим кольцом с тремя гидрофобными радикалами фермента (остатки аминокислот изолейцина, тирозина и глутамина).
 |
Смотрите также
Никелирование и хромирование
...
Губчатые изделия
Тема данной курсовой работы «Губчатые изделия», эта тема довольно
актуальна, так как производство губчатых изделий занимает не маловажное место в
промышленности. Потому что эти изделия имеют ...
Замена углерода
Ученые немало
высказывались на тему возможности построения органических молекул с помощью
других атомов, но на практике доказать эту возможность на данный момент не
удалось.
...


