Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Гибридизация орбиталейСтатьи и работы по химии / Статьи и работы по химии / Гибридизация орбиталей Гибридизация орбиталейСтраница 1
Вращательные движения определяют важнейшие черты стационарных состояний электронных оболочек и ядер aтомов и молекул. Некоторые приемы теоретического анализа состояний атомно-молекулярных систем особенно наглядно можно исследовать на примере простейшей модели вращения – плоского ротатора. Мы уже рассмотрели замену комплексных орбиталей действительными волновыми функциями, допускающими наглядное графическое представление. Следующий прием - построение гибридных орбиталей, каждая из которых уже не обладает центральной симметрией, а напротив, отличается ярко выраженной концентрацией в некотором выделенном направлении. Заглядывая вперед, отметим, что гибридные электронные орбитали атомов играют важнейшую роль в образовании химических связей.
Эффект гибридизации позволяет наглядно проиллюстрировать применение принципа суперпозиции состояний, чрезвычайно важного для химии и для всей квантовой механики.
Гибридизация – это смешение состояний с различными значениями момента импульса. Например, гибридные орбитали можно образовать из волновых функций σ- и π-типа, но из орбиталей только π-типа – нельзя.
Смешивая орбитали разных уровней, удается построить гибкие формы орбиталей, пригодные для описания каких-либо физических или химических явлений, рассмативая их как возмущение исходных состояний системы. С этой целью образуют линейные комбинации из волновых функций, принадлежащих различным уровням. Энергии гибридизующихся орбиталей различаются, но это отличие должно быть невелико.
На основе исходного набора волновых функций – тройки орбиталей (![]() ), принадлежащих двум низшим ypoвням плоского ротатора, возможны два предельных способа построения гибридов. В первом из них гибридизуются только σ- и лишь одна из двух π-орбиталей, тогда как вторая остается несмешанной. Например, образуем ниже гибрид из σ- πс, не затрагивая πs. Назовем этот тип смешения σπ-гибридизацией. Во втором случае смешиваются все три исходные орбитали, т.е. происходит σπ2-гибридизация. Число гибридных функций всегда равно числу исходных смешивающихся орбиталей.
), принадлежащих двум низшим ypoвням плоского ротатора, возможны два предельных способа построения гибридов. В первом из них гибридизуются только σ- и лишь одна из двух π-орбиталей, тогда как вторая остается несмешанной. Например, образуем ниже гибрид из σ- πс, не затрагивая πs. Назовем этот тип смешения σπ-гибридизацией. Во втором случае смешиваются все три исходные орбитали, т.е. происходит σπ2-гибридизация. Число гибридных функций всегда равно числу исходных смешивающихся орбиталей.
В обоих случаях исходные орбитали образуют ортонормированный базисный набор (2.4) или кратко базис, и в этом смысле совершенно подобны некоторым единичным векторам. Орбитали базисного набора удобно представить в упорядоченном виде вектора-столбца или вектора-строки, вводя при этом унифицированные обозначения
![]() ,
,
или равноценно
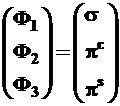 , где
, где ![]()
Образование гибридных орбиталей представляет собой смешение исходных базисных орбиталей, т.е. их линейную комбинацию. Численные коэффициенты при базисных функциях определяют их вклады в составе гибрида и, как правило, находятся из простых соображений.
Возможные варианты образования ортонормированных гибридных орбиталей представим схемой:
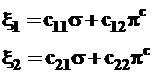 (3.42)
(3.42) 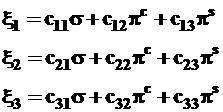 (3.43)
(3.43)
В матричной форме эти выражения примут вид:
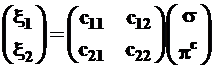
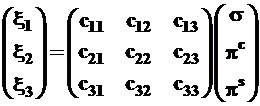 (3.44)
(3.44)
Для каждой из гибридных i-орбиталей алгебраическая связь между коэффициентами при компонентах ортонормированного базиса (в нашем случае ![]() ) идентична обычной связи между проекциями ортонормированных векторов:
) идентична обычной связи между проекциями ортонормированных векторов:
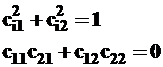 для i=1, 2
для i=1, 2 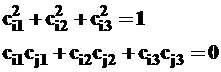 i=1, 2, 3, j ≠ i
i=1, 2, 3, j ≠ i
Согласно постулату 4 (уравнение 2.29) квадраты коэффициентов наделены определенным смыслом. Каждый из них определяет вероятность “чистого” исходного состояния в составе смешанного.
Для простоты и определенности образуем такие гибриды, при смешении 2-х волновых функций (σ и πс), вес каждой из них в составе гибридных орбиталей одинаков, т.е. равен 1/2:
![]() .
.
Последнее соотношение приводит к выводу:
![]() (3.45)
(3.45)
откуда для разных значений i=1, 2 получаем равноценные возможности, т.е. два вектора
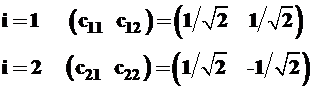
Следовательно, гибридные орбитали имеют вид:
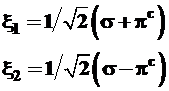 (3.46)
(3.46)
Подставив в (3.46) явные выражения базисных векторов (336) и (3.40), получим гибридные орбитали как функции полярного аргумента:
![]() (3.47)
(3.47)
Смотрите также
Характеристика элементов подгруппы азота
...
Переработка каучуков
Резиновые смеси на основе
фторкаучуков изготовляют и перерабатывают на обычном оборудовании. Из-за
повышенной жесткости каучуков и резиновых смесей и их сильного разогрева при
обработке загрузка об ...
Определение жесткости воды комплексонометрическим методом
В природных водах
находится очень большое количество различных химических соединений. В процессе
естественного кругооборота природные воды, находясь в контакте с воздухом и
породами земной ...


