Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Равновесные диаграммы потенциал-pH (диаграммы Пурбе или диаграммы электрохимического равновесия).
Принципы построения. Использование диаграмм ПурбеДипломы, курсовые и прочее / Равновесные и поляризационные диаграммы потенциал-pH / Дипломы, курсовые и прочее / Равновесные и поляризационные диаграммы потенциал-pH / Равновесные диаграммы потенциал-pH (диаграммы Пурбе или диаграммы электрохимического равновесия).
Принципы построения. Использование диаграмм Пурбе Равновесные диаграммы потенциал-pH (диаграммы Пурбе или диаграммы электрохимического равновесия).
Принципы построения. Использование диаграмм ПурбеСтраница 2
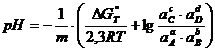 (1.3.10)
(1.3.10)
М. Пурбе описал пять основных приложений равновесных диаграмм pH-потенциал чистых металлов:
1) теоретическое обоснование областей или условий коррозии (самопроизвольного растворения), иммунности (термодинамической устойчивости) и пассивации (условий, при которых термодинамически неустойчивые металлы практически не подвергаются растворению вследствие кинетических затруднений);
2) оценка стойкости металлов в воде;
3) установление металлов, которые находятся в активном или пассивном состоянии в определенной коррозионной среде;
4) оценка возможностей использования окисляющих ингибиторов коррозии (хроматов, молибдатов и т.д.);
5) классификация металлов по степени их благородности (термодинамической устойчивости) [3].
Вследствие диссоциации воды в водных растворах всегда присутствуют ионы водорода и гидроксила. Поэтому на всех электродах может протекать не только собственно электродная реакция, но и реакции, проходящие на водородном и кислородном электродах. Таким образом, теоретически в водных растворах электроды всегда рассматриваются как смешанные.
Смотрите также
Модификация неорганических мембран нанокристаллитами пироуглерода
В настоящее время
мембранное разделение жидких и газообразных смесей достаточно широко
используется в различных отраслях промышленности. Наряду с очевидными
достоинствами этого метода разде ...
Основы метода потенциометрического
титрования.
Рассмотрим основные
понятия потенциометрического титрования, его виды и методы проведения, способы установления
точки эквивалентности при титровании. ...


