Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Электролиты. Коллигативные свойства растворов электролитовДипломы, курсовые и прочее / О растворах / Дипломы, курсовые и прочее / О растворах / Электролиты. Коллигативные свойства растворов электролитов Электролиты. Коллигативные свойства растворов электролитов
Электролиты – это вещества, растворы которых проводят электрический ток посредством ионов, на которые они распадаются под действием полярных молекул растворителя.
Количественной характеристикой диссоциации электролита является степень диссоциации ![]() , которая равна отношению числа продиссоциировавших молекул к общему числу молекул:
, которая равна отношению числа продиссоциировавших молекул к общему числу молекул:
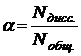
По степени диссоциации различают сильные электролиты ![]() слабые электролиты
слабые электролиты ![]() и электролиты средней силы
и электролиты средней силы ![]()
Коллигативными называются свойства растворов, которые не зависят от природы растворенного вещества, а только от его концентрации. Такие свойства проявляются в полной мере в идеальных растворах.
Идеальными называются растворы, при образовании которых не происходит изменения энтальпии и объема системы, не идут химические реакции между компонентами, а силы межмолекулярного взаимодействия между всеми компонентами одинакова. Наиболее близки к идеальным – разбавленные растворы неэлектролитов.
Для бесконечно разбавленных растворов, состояние которых близко к состоянию идеальных, такими свойствами являются:
– осмотическое давление;
– понижение давления насыщенного пара над раствором;
– повышение температуры кипения;
– понижение температуры замерзания раствора.
Изучение коллигативных свойств разбавленных растворов используется для определения молярной массы растворенного вещества, а также его степени диссоциации или показателя ассоциации.
Смотрите также
Дериватографический анализ пирита
5-секундная активация
пирита приводит к заметному увеличению площади экзотермы, уменьшению
температурного интервала окисления и большей потере массы при нагревании.
Увеличение времени обработки в п ...
Физико-химия конкретных промышленных каталитческих процессов
Окислительный аммонолиз пропилена.
Окислительное хлорирование этилена. Основные особенности процессов окисления в
псевдоожиженном слое катализатора. «Воздушный» и «кислородный» процессы. Рец ...
Ознакомление с некоторыми операциями
лабораторной практики и измерительными приборами.
Цель
работы - ознакомление студентов с взвешиванием, измерением объемов жидкостей,
титрованием и др., а также с некоторыми химическими и измерительными приборами.
При подготовке к
выполнению ла ...


