Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Качественная реакция на кобальт (Со)Дипломы, курсовые и прочее / Методы контроля и анализа веществ (химические методы) / Дипломы, курсовые и прочее / Методы контроля и анализа веществ (химические методы) / Качественная реакция на кобальт (Со) Качественная реакция на кобальт (Со)
Решение:
Кобальт можно идентифицировать, переведя его из пробы в раствор в виде ионов Co2+ по реакции
3Co + 8HNO3 (разбавленная, горячая) = 3Co(NO3)2 + 2NO↑ + 4H2O
После этого можно проводить качественные реакции на ионы Co2+.
1) Действие реагента Ильинского (1-нитрозо-2-нафтола):
В реакции Co2+ с реагентом Ильинского при участии растворимого кислорода получается нерастворимое темно-красное хелатное соединение кобальта (III):
Co2+ + 12C10H6(NO)OH + O2 = 4[C10H6(NO)O]3Co↓ + 2H2O + 8H+
Строение комплексного соединения такое:
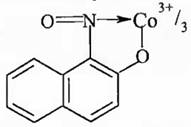
Осадок [C10H6(NO)O]3Co не растворяется в кислотах и щелочах. Идентификацию Co2+ проводят в кислой среде. Мешают ионы Cu2+, Fe3+, Fe2+.
2) Качественная реакция на ионы Co2+ с образованием кобальтонитрита (III) калия:
Нитрит калия образует с ионами Co2+ в уксуснокислом растворе при pH 4 – 5 желтый кристаллический осадок состава K3[Co(NO2)6]. Образованию осадка предшествует окисление Co2+ нитритом:
Co2+ + NO2- + 2H+ = Co3+ + NO↑ + H2O
Суммарный процесс можно показать уравнением:
Co2+ + 7NO2- + 3K+ + 2H+ = K3[Co(NO2)6]↓ + NO↑ + H2O
В разбавленных растворах осадок образуется при нагревании и отстаивании. Реакцию часто используют для отделения кобальта от мешающих ионов. Граница определения кобальта – 0,4 мкг.
Смотрите также
Понятие и биологическая роль ферментов
Я выбрала тему «Ферменты.
Биокатализ. Возможности биомиметики», потому что в последнее время в качестве
лекарственных средств стали широко применять препараты, оказывающие
направленное влия ...
Изучение механизма изомеризационной рециклизации методом молекулярной механики
В последние годы
круг соединений, способных к рециклизации, расширился за счет производных
пиридиниевых солей с цианидными, карбонильными, сложноэфирными и мостиковыми
полиметиленовыми заме ...
Использование озона
Озон -
высокоэффективное и универсальное окисляющее вещество, которое используется в
обработке воды в целях дезинфекции, удаления марганца и железа, улучшения
вкуса, устранения цвета и запа ...


