Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Растворы сильных электролитовОткрытая химия / Растворы / Открытая химия / Растворы / Растворы сильных электролитов Растворы сильных электролитовСтраница 2
Здесь C – аналитическая концентрация, z – заряд катиона или аниона. Для одно-однозарядного электролита ионная сила совпадает с концентрацией. Таким образом, NaCl и Na2SO4 при одинаковых концентрациях будут иметь разные ионные силы. Сопоставление свойств растворов сильных электролитов можно проводить только тогда, когда ионные силы одинаковы; даже небольшие примеси резко изменяют свойства электролита.
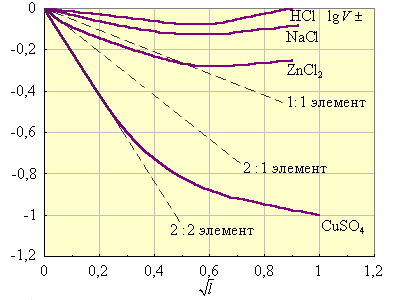
На рис. 6.6 сопоставляются вычисленные и экспериментальные значения lg γ± при различных ионных силах. Из него видно, что уравнение Дебая–Хюккеля выполняется только для разбавленных растворов.
 |
|
Рисунок 6.6 Зависимость |
Пунктирные прямые рассчитаны по уравнению Дебая–Хюккеля. Знание коэффициентов активностей позволяет оценить реальные свойства сильных электролитов.
Смотрите также
Интересные и опасные свойства ртути
...
Белки молока, строение и функции
В жизни человека наиболее важную роль играет питание.
Оно определяет и физическое состояние, а также физическое и умственное
развитие, повышает иммунитет и т. д.
Молока считается наиболее ...
Фтор
ФТОР (лат. Fluorum), F, химический элемент с атомным
номером 9, атомная масса 18,998403. Природный фтор состоит из одного
стабильного нуклида 19F. Конфигурация внешнего электронного слоя 2s2 ...


