Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Гомогенное газофазное окисление этилена
в окись этиленаУчим химию / Окись этилена / Учим химию / Окись этилена / Гомогенное газофазное окисление этилена
в окись этилена Гомогенное газофазное окисление этилена
в окись этиленаСтраница 1
При прямом гомогенном окислении этилена кислородом образуется ряд ценных продуктов: окись этилена, формальдегид, органические кислоты. сейчас разрабатываются методы синтеза окиси этилена гомогенным окислением этилена в газовой фазе, так как для этого процесса не требуется затрат ни дорогого катализатора, ни хлора. Кроме того, при этом способе получения окиси этилена не требуются этилен и воздух такой высокой степени очистки, как при каталитическом окислении этилена. К недостаткам этого метода относятся многообразие образующихся продуктов и низкая селективность, что объясняется цепной природой происходящих превращений и высокой температурой. Однако развитие теории цепных процессов открывает новые пути совершенствования реакций газофазного окисления этилена.
Рассмотрим влияние условий на процесс образования окиси этилена. Первым фактором мы рассмотрим влияние температуры.
При температуре ниже 300°С этилен не взаимодействует с кислородом, медленное окисление начинается при 300°С ![]() . С повышением температуры скорость процесса резко возрастает. Оптимальной температурой считают ту, при которой 65% поданного в зону реакции кислорода вступает во взаимодействие с этиленом.
. С повышением температуры скорость процесса резко возрастает. Оптимальной температурой считают ту, при которой 65% поданного в зону реакции кислорода вступает во взаимодействие с этиленом.
При температуре ниже 400°С степень превращения кислорода за один проход составляет примерно 35%. При температуре выше 550°С резко возрастает скорость окисления этилена до двуокиси углерода и воды, а скорость образования окиси этилена уменьшается.
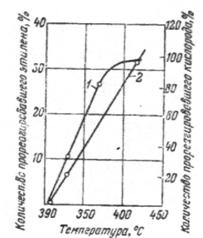
Рис. 2.3. Влияние температуры на глубину окисления этилена.
На рис. 2.3 представлена температурная зависимость степени превращения исходных компонентов при прямом окислении этилена. Состав исходной смеси – 80% С2Н4 и 12% О, время реакции 20 сек; стеклянный реактор длиной ~500 мм и диаметром 46 мм. Из рассмотрения кривых, представленных на рис. 2.3 можно сделать выводы:
1. С ростом температуры степень конверсии этилена возрастает.
2. Количество реагирующего кислорода сначала быстро растет с повышением температуры – при 360°С в реакцию вступает более 80% исходного кислорода. Выше этой температуры кривая расхода кислорода резко изменяет свой наклон и асимптотически приближается к 100% ![]() .
.
В данном процессе возможно протекание нескольких побочных реакций. В частности возможно при температурах 320 - 335ºС образование формальдегида:
![]()
Другой побочной реакцией, которая может идти в этих условиях, является образование бирадикала диметиленоксида и дальнейшее его взаимодействие с этиленом с образованием пропилена и формальдегида:
![]()
Такой процесс наблюдался при взаимодействии окиси этилена с этиленом при температурах выше 400°С. При температурах ниже 350°С образование пропилена не происходило ![]() .
.
Исследования показали влияние на процессы окисления этилена добавления небольших количеств озона, который ускорял процессы окисления. Это можно считать доказательством цепного механизма окисления этилена в окись этилена ![]() .
.
Смотрите также
Тантал
В честь древнего героя
Тантала назван металл, значение которого в наши дни неизменно растет. С каждым
годом расширяется круг его применений, а вместе с этим и потребность в нем.
Однако руды его ре ...
Свойство водных растворов
электролитов.
Цель
работы:
ознакомится с электропроводностью растворов, ионными равновесиями в растворах
электролитов.
Согласно
теории электролитической диссоциации электролиты при растворении в воде
распад ...
Получение гидроксида натрия каустификацией содового раствора
Гидроксид натрия (каустическая сода) используется
во многих отраслях промышленности: химической, металлургической, нефтеперерабатывающей,
мыловаренной, фармацевтической, целлюлозно-бумажной, ...


