Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Взаимодействие a-литиированных
альдонитронов с С-электрофилами. Взаимодействие
с a,b-ненасыщенными карбонильными соединениями.Библиотека / Реакции a-литиированных циклических нитронов с электрофильными реагентами / Библиотека / Реакции a-литиированных циклических нитронов с электрофильными реагентами / Взаимодействие a-литиированных
альдонитронов с С-электрофилами. Взаимодействие
с a,b-ненасыщенными карбонильными соединениями. Взаимодействие a-литиированных
альдонитронов с С-электрофилами. Взаимодействие
с a,b-ненасыщенными карбонильными соединениями.Страница 2
. [xxxix]
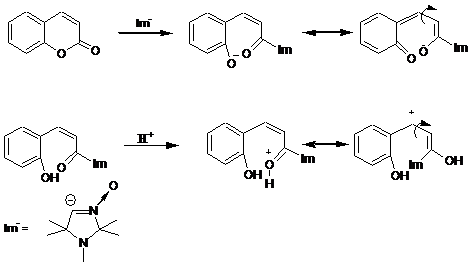
Изменение конфигурации двойной связи может происходить как после присоединения нуклеофильного реагента к сопряжённой карбонильной группе, так и во время обработки реакционной смеси кислотой.
При взаимодействии соединения 65
с иодистым метилом в ацетоне в присутствии поташа происходит практически количественное образование продукта алкилирования по фенольной группе 67
. В спектре ЯМР 1Н полученного соединения отсутствует сигнал спиртовой группы, но присутствует сигнал группы ОСН3 при 3.66 м.д.
Спектр ЯМР 13С полученного продукта алкилирования практически полностью совпадает с ЯМР 13С спектром соединения 65
за исключением появления сигнала при 55.48 м.д., отнесённого к резонансу атома углерода группы ОСН3.
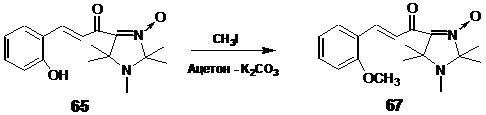
Аналогично, литиирование альдонитрона ряда пирролин-1-оксида 59
s-BuLi при -70 0С и последующая обработка раствором кумарина в диэтиловом эфире привели к образованию 3-(2-гидроксифенил)-1-(3,3,5,5-тетраметилпирролин-1-оксид-2-ил)пропенона 65a
. Взаимодействие металлированного альдонитрона ряда 3,4-дигидроизохинолин-2-оксида 61
с кумарином в указанных выше условиях привело к образованию 1-(3,3-диметил-3,4-дигидроизохинолин-2-оксид-1-ил)-3-(2-гидроксифенил)пропенона 65б
с выходом 25 %. На основании данных спектроскопии ЯМР 1Н было установлено, что соединения 65а
и 65б
также обладают транс-конфигурацией двойной связи.
Нами исследовано взаимодействие металлированного альдонитрона 58
c 1-фенил-2-диметиламинометил-пропен-2-оном-1 68
. Реакция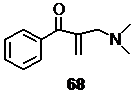 с выходом 60% приводит к образованию соединения, в спектре ЯМР 1Н которого присутствуют сигналы 4 геминальных метильных групп при 1.01, 1.43, 1.46, 1.49 м.д., два сигнала с соотношением интегральных интенсивностей 2:1 при 2.26 и 2.29 м.д., отнесённые к резонансу атомов водорода соответственно групп N-(CH
с выходом 60% приводит к образованию соединения, в спектре ЯМР 1Н которого присутствуют сигналы 4 геминальных метильных групп при 1.01, 1.43, 1.46, 1.49 м.д., два сигнала с соотношением интегральных интенсивностей 2:1 при 2.26 и 2.29 м.д., отнесённые к резонансу атомов водорода соответственно групп N-(CH
3)2 и N-CH
3, и сигналы ароматических протонов в областях 7.2-7.4 м.д. и 7.5-7.6 м.д. Мультиплет с центром при 3.09 м.д., представляющий собой АВ-систему, был отнесен к резонансу протонов фрагмента H-C-H (2J = 12 Гц), два синглета при 4.55 и 5.00 м.д. были отнесены к резонансу атомов водорода группы С=СH
2, а уширенный сигнал в области 7.7 - 8.0 м.д. (в CDCl3) был отнесён к резонансу атома водорода ОНгруппы. Таким образом, на основании спектральных данных и данных элементного анализа полученному соединению была приписана структура 2-диметиламинометил-1-(1,2,2,5,5-пентаметил-3-имидазолин-3-оксид-4-ил)-1-гидрокси-l-фенилпропена-2 69
.
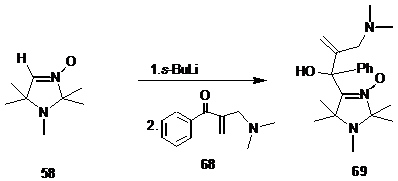
Аналогично, в указанных выше условиях реакция литиированного нитрона 59
с соединением 68приводит к образованию 2-диметиламинометил-1-(3,3,5,5-тетраметил-пирролин-1-оксид-4-ил)-1-гидрокси-l-фенилпропена-2 69а
с выходом 75 %.
Таким образом, взаимодействие литиированных производных альдонитронов с a,b-ненасыщенными карбонильными соединениями проходит исключительно по карбонильной группе. Образование продуктов 1,4-нуклеофильного присоединения не наблюдается, что в общем характерно для литийорганических соединений.


