Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Молекулярные орбитали метанаОрганическая химия / Внутри- и межмолекулярные взаимодействия / Органическая химия / Внутри- и межмолекулярные взаимодействия / Молекулярные орбитали метана Молекулярные орбитали метанаСтраница 2
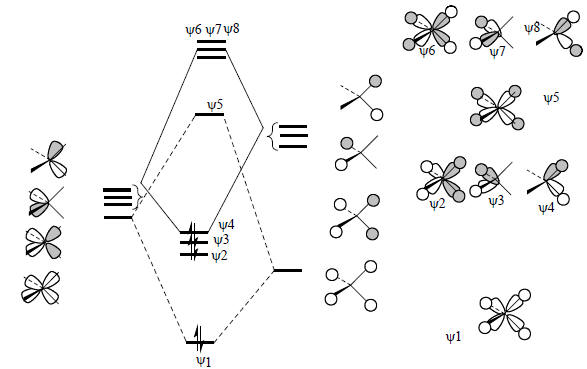 Рис. 2.20. Делокализованные гибридные орбитали молекулы метана
Рис. 2.20. Делокализованные гибридные орбитали молекулы метана
Как отмечалось выше, плоский метан нестабилен потому, что групповая орбиталь ψ4 не участвует в связывании. Если бы эта орбиталь сильно возмущалась, то ее нижний возмущенный уровень мог бы уйти ниже уровня орбитали pz, и тогда в связывании четырех атомов углерода участвовало бы уже на 6, а 8 электронов. Это возможно в аналогах метана АН4, в которых центральный атом А имеет доступные (т.е. относительно низко лежащие) d-орбитали, та как симметрия d -орбиталей (два угловых узла) как раз подходит к симметрии орбитали ψ4:
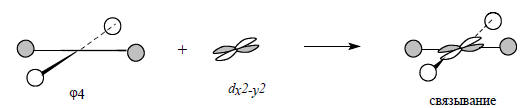
Действительно, неэмпирический расчет показывает, что в ряду CH4, SiH4, GeH4, SnH4, TiH4 энергия плоских форм молекул постепенно и значительно понижается, поскольку d-орбитали становятся все более и более доступными (по энергии) для эффективного взаимодействия с ψ4. В молекуле пустые d- орбитали титана очень эффективно связывают атомы водорода и рассчитанные энергии плоской квадратной и тетраэдрической форм мало отличаются между собой.Вторым важным фактором является увеличения размеров центрального атома. Чем больше атомный радиус, тем дальше отстоят друг от друга атомы водорода, т.е. тем больше размеры групповой орбитали Н4. Это понижает энергию орбитали ψ4, так как в ней все взаимодействия между соседними атомами водорода антисвязывающие. Эффект заметен в случае плоского силана SiH4, в котором пустые d-орбитали кремния еще лежат достаточно высоко и в связывании практически не участвуют.Орбиталь ψ1 (рис. 2.20) имеет более низкую энергию, чем вырожденные орбитали ψ2, ψ3 и ψ4, поскольку у нее нет узлов, и, следовательно, с нее труднее удалить электрон.
Смотрите также
Использование озона
Озон -
высокоэффективное и универсальное окисляющее вещество, которое используется в
обработке воды в целях дезинфекции, удаления марганца и железа, улучшения
вкуса, устранения цвета и запа ...
Радиометрическая и радиохимическая экспертиза
...
Сорбируемость меди на бурых углях, сапропелях и выделенных из них гуминовых кислотах
Проблема очистки воды для хозяйственно - питьевых нужд от
токсикантов, в частности, от соединений тяжелых металлов, является весьма
актуальной природоохранной проблемой в Тульском регионе, в ...


