Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Понятие об активной кислотности.Библиотека / Определение содержания аскорбиновой кислоты в яблоках различных сортов / Библиотека / Определение содержания аскорбиновой кислоты в яблоках различных сортов / Понятие об активной кислотности. Понятие об активной кислотности.
Вода и водные растворы диссоциирующих веществ в той или иной степени ионизированы. В воде непрерывно протекает процесс диссоциации воды на водородный и гидроксильный ионы и рекомбинация этих ионов в недиссоциированные молекулы воды. Скорость распада воды на ионы пропорциональна действующей массе реагирующих молекул воды, а скорость рекомбинации воды пропорциональна произведению действующих масс реагирующих ионов. Это состояние выражается формулой
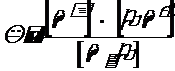 ,
,
где К – константа диссоциации, а символы в квадратных скобках – концентрации соответствующих ионов и молекул.
Кислоты в водных растворах диссоциируют на водородный ион и отрицательно заряжнный остаток кислоты. Сильные кислоты почти нацело диссоциированы на ионы, а слабый – диссоциированы в слабой степени. Наприме, 0.1 н. раствора HCl диссоциирован на 91 %, а такой же раствор уксусной кислоты только на 1.36%. Следовательно, сила кислот зависит не от общего количества находящегося в них водорода, а только от ионов водорода. От концентрации водородных ионов зависит истинная кислотность или щелочность среды.
В настоящее время принято обозначать концентрацию водородных ионов символом рН для растворов не крепче нормального. Численное выражение рН представляет собой десятичный логарифм числа, показывающего количество граммов водородных ионов в 1л. При этом отрицательный знак опущен.
Смотрите также
Получение метана и опыты с ним
...
Выводы.
1. Отработана методика получения безводного
трихлорида самария.
2. Изучен механизм электровосстановления
иона самария в хлоридных и хлоридно-фторидных расплавах.
3. Показано, что для ...


