Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Порядок реакции по реагенту А2Статьи и работы по химии / Исследование кинетики реакции / Определение вида кинетического уравнения и порядков реакции
по реагентам / Статьи и работы по химии / Исследование кинетики реакции / Определение вида кинетического уравнения и порядков реакции
по реагентам / Порядок реакции по реагенту А2 Порядок реакции по реагенту А2Страница 1
Выбираем опыты, в которых начальная концентрация реагента А2 изменяется, а концентрация А1 постоянна. Эти данные приведены в таблице 7.
Таблица 7.
Начальные концентрации и скорости, и их логарифм для опытов №9,№8,№2,№4,№5.
|
опыт |
Rнач,моль/л*мин |
C02,моль/л | ||
|
0 |
0 |
0 |
0 |
0 |
|
3 |
0.079 |
0,4 |
-0.699 |
-1.1024 |
|
4 |
0.147 |
0,6 |
-0.3979 |
-0.832684 |
|
5 |
0.24 |
0,6 |
-0.2218 |
-0.61979 |
|
По данным таблицы 7 строим график зависимости |
, который представлен на рисунке 5.
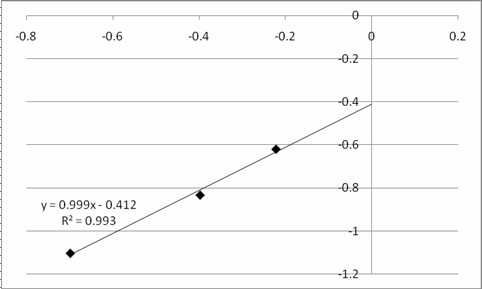
|
Рис. 5. График зависимости |
.
|
Порядок реакции по реагенту А2 определяем как тангенс угла наклона линии аппроксимации. |
, следовательно порядок реакции по реагенту А2 равен 1.
Определим порядок по реагенту А2. интегральным методом. По предыдущему расчету определили, что порядок реакции по данному компоненту первый. Тогда кинетическое уравнение будет иметь вид:
|
Интегрируя его и учитывая начальное условие (при t=0, C2=C02), получаем уравнение: |
|
. Данное уравнение представляет собой уравнение прямой в координатах . Зависимости |
для каждого опыта представлены на рисунках 6-9.
|
Опыт №1. Зависимость |
.
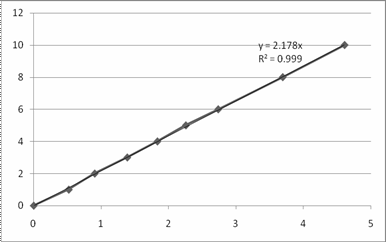
|
Опыт №2. Зависимость |
.
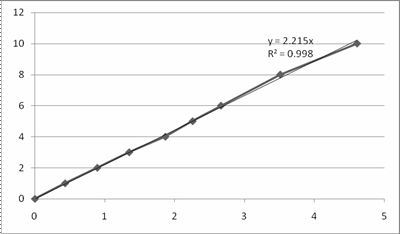
|
Опыт №3. Зависимость |
.
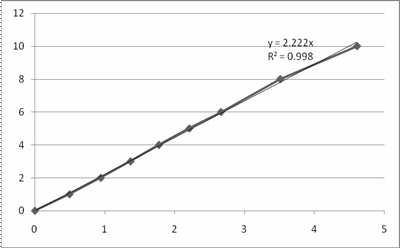
|
Рис. 6. Графики зависимости |
для опытов 1-3.
|
Опыт №4. Зависимость |
Смотрите также
Равновесные и поляризационные диаграммы потенциал-pH
В настоящее время
большую важность имеет возможность оценивать устойчивость металлов и их сплавов
к коррозии в тех или иных условиях. Эту возможность позволяет реализовать на
практике приме ...
Реакторный графит: разработка, производство и свойства
Конструкционные
углеродные материалы (КУМ) нашли широкое применение в атомных реакторах
различного назначения: исследовательских, транспортных, промышленных
уран-графитовых (ПУГР), высокоте ...
Осмий - благородный металл
ОСМИЙ
(лат. Osmium), Os, химический элемент VIII группы периодической системы,
атомный номер 76, атомная масса 190,2, относится к платиновым металлам.
...


