Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Расчет ректификационной колонны. Расчет материального балансаДипломы, курсовые и прочее / Расчет ректификационной колонны / Дипломы, курсовые и прочее / Расчет ректификационной колонны / Расчет ректификационной колонны. Расчет материального баланса Расчет ректификационной колонны. Расчет материального балансаСтраница 1
Уравнения материального баланса ректификационной колонны непрерывного действия, учитывающее количество поступающих и уходящих потоков, имеет следующий вид:
GF = GD +GW (1)
где GF – количество поступающей на разделение смеси, кг/с;
GD – массовый расход дистиллята, кг/с;
GW – массовый расход кубового остатка, кг/с;
GF∙ХF = GD∙ХD +GW∙ХW (2)
где ХD – концентрация низкокипящего компонента в дистилляте, массовые доли;
ХW – концентрация низкокипящего компонента в кубовом остатке, массовые доли;
ХF – концентрация низкокипящего компонента в исходной смеси, массовые доли.
Для того, чтобы найти массовый расход дистиллята ХD и массовый расход кубового остатка ХW подставим исходные данные в уравнение (1) и в уравнение (2). Затем решим эти уравнения совместно.
GD +GW = 10000
GD ∙ 0,995 + GW ∙ 0,3 = 10000 ∙ 0,9
GD ∙ 0,995 + (1000-GD) ∙ 0,3 = 9000
0,695 ∙ GD = 9000 − 3000
0,695 ∙ GW = 6000
GD =8633 кг/ч
GD = 10000 − 8633 = 1367 кг/ч
Массовый расход дистиллята: GD = 8633 кг/ч
Массовый расход кубового остатка: GW =1367 кг/ч
Для дальнейших расчетов выразим концентрации питания, дистиллята и кубового остатка в мольных долях.
Содержание низкокипящего компонента в питании вычисляют по формуле:
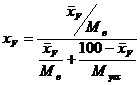 (3)
(3)
где ХF – концентрация низкокипящего компонента в питании, мольные доли;
Мв – мольная масса низкокипящего компонента, кг/моль;
Мукс – мольная масса высококипящего компонента, кг/моль;
Мукс = 60 кг/кмоль;
Мв = 18 кг/кмоль;
Содержание низкокипящего компонента в дистилляте вычисляют по формуле:
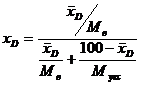 (4)
(4)
где ХD - концентрация низкокипящего компонента в дистилляте, мольные доли
Содержание низкокипящего компонента в кубовом остатке вычисляют по формуле:
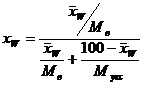 (5)
(5)
![]()
где ХW - концентрация низкокипящего компонента в кубовом остатке, мольные доли.
Подставим в формулу(3), в формулу (4) и в формулу (5) исходные данные и найдем содержание уксусной кислоты в смеси (питании), в дистилляте и в кубовом остатке.
ХF = 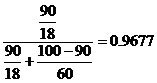
ХD = 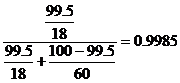
ХW = 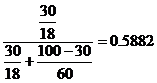
Относительный мольный расход питания определяется по уравнению:
![]() (6)
(6)
![]()
Для проведения дальнейших расчетов нам необходимо построить кривую равновесия в координатах ![]() для системы этиловый спирт-вода при атмосферном давлении.
для системы этиловый спирт-вода при атмосферном давлении.
Здесь ![]() - мольные доли воды в жидкости и в равновесном с ним паре.
- мольные доли воды в жидкости и в равновесном с ним паре.
РБ и РТ – давление насыщенного пара воды и уксусной кислоты соответственно П- общее давление
![]()
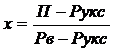
![]()
Все необходимые данные для построения кривой равновесия приведены в таблице 1.
Таблица 1. Равновесные составы жидкости и пара для системы Уксусная кислота - вода
|
t, °C |
x |
y |
|
118,1 |
0 |
0 |
|
115,4 |
0,05 |
0,092 |
|
113,8 |
0,1 |
0,167 |
|
110,1 |
0,2 |
0,302 |
|
107,5 |
0,3 |
0,425 |
|
105,8 |
0,4 |
0,53 |
|
104,4 |
0,5 |
0,626 |
|
103,2 |
0,6 |
0,716 |
|
102,1 |
0,7 |
0,795 |
|
101,3 |
0,8 |
0,864 |
|
100,6 |
0,9 |
0,93 |
|
100 |
1 |
1 |
Смотрите также
Азотные,калийные,фосфорные удобрения
...
Гидразид изоникотиновой кислоты, его производные и аналоги
...
Антибиотики
Антибиотики, вырабатываемые микроорганизмами химические вещества, которые способны тормозить рост и вызывать гибель бактерий и других микробов. Противомикробное действие антибиотиков имеет избирательн ...


