Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Химические свойства аллилового спиртаДипломы, курсовые и прочее / Получение аллилового спирта гидролизом хлористого аллила / Дипломы, курсовые и прочее / Получение аллилового спирта гидролизом хлористого аллила / Химические свойства аллилового спирта Химические свойства аллилового спирта
Аллиловый спирт, имея в молекуле кратную связь и гидроксильную группу, проявляет свойства спиртов и непредельных соединений:
1. Взаимодействие с галогенами с образованием β - дигалоидгидринов глицерина
Совершенно иначе, чем этиловый спирт, относится аллиловый спирт к хлору и брому; тогда как обыкновенный спирт дает с ними продукты замещения и окисления (напр. хлораль), аллиловый спирт прямо присоединяет два атома хлора, брома или йода, образуя β-дигалоидгидрины глицерина C3H6Cl2O, C3H6Br2O и C3H6J2O [2]:
![]() ,
,
2,3-дибромпропанол-1
![]() .
.
2,3-дихлорпропанол-1
2. Реакция гидрирования [10]:
![]() .
.
пропанол-1
3. Реакция гидратации в присутствии кислорода с образованием глицерина [24]:
![]() .
.
глицерин
4. Окисление с образованием альдегида [24]
Окислителями переводится в альдегид - акролеин, дальнейшее окисление дает акриловую кислоту:
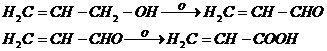 .
.
5. Взаимодействие со щелочными металлами с образованием алкоголятов [10]
Со щелочными металлами получаются алкоголяты, которые при действии хлористого аллила дают соответствующий этиловому эфиру аллиловый эфир (С3Н5)2О:
![]() ,
,
алкоголят
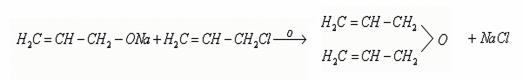
6. Межмолекулярная дегидратация спиртов с образование простых эфиров [27]:
![]() .
.
этилаллиловый эфир
7. Взаимодействие с минеральными и органическими кислотами с образованием сложных эфиров
Образование сложных эфиров происходит при взаимодействии с минеральными и органическими кислотами [26]:
![]() ,
,
аллилацетат
![]() .
.
8. Взаимодействие с магнийгалогеналкилами
Происходит замещение гидроксильного водорода на магнийгалоген и выделение углеводорода [10]:
![]() .
.
9. Взаимодействие с хлористым фосфором - PCl3 [31]
Треххлористый фосфор дает хлористый аллил C3H5Cl, изомерный с α- и β – хлорпропиленами:
![]() .
.
Аналогичным путем образуется йодистый аллил C3H5J:
![]() .
.
10. Гидратация под действием слабых минеральных кислот
При действии слабых минеральных кислот аллильный спирт способен присоединять элементы воды, причем превращается в пропиленгликоль который, вновь теряя воду, переходит уже в изомерный с аллиловым спиртом пропионовый альдегид или его продукты конденсации [24]:
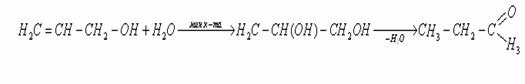
Смотрите также
Фосфор и его соединения
Фосфор (лат. Phosphorus)
P – химический элемент V группы периодической системы
Менделеева атомный номер 15, атомная масса 30,973762(4). Рассмотрим строение
атома фосфора. На наружном энерге ...
Алкалоиды
...
Биохимия
Не вдаваясь в подробности происходящих в живых организмах
процессах, отметим, что эти процессы возможны только при использовании внешних
источников энергии и питательных веществ: для растений первич ...


