Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Полярные молекулы.Статьи и работы по химии / Атомно-молекулярное учение и его законы / Химическая связь и строение молекул. / Статьи и работы по химии / Атомно-молекулярное учение и его законы / Химическая связь и строение молекул. / Полярные молекулы. Полярные молекулы.Страница 1
При рассмотрении химической связи с точки зрения взаимодействия двух ядер и образования общей для них электронной пары нельзя провести резкую границу между ионной и ковалентной связями. Если молекула образована одинаковыми атомами, общая электронная пара принадлежит обоим атомам в равной мере и оба атома электрически нейтральны. Однако в тех случаях, когда молекула состоит из различных атомов, связующая электронная пара обычно смещена в сторону одного из них, а именно в сторону того атома, который обладает бульшим сродством к электрону. Например, в соединениях галогенов с водородом общая электронная пара смещена в направлении атома галогена, в результате чего та часть молекулы, в которой находится галоген, приобретает некоторый частичный отрицательный заряд, а противоположная, где находится водород, заряжается частичным положительным зарядом. Однако наличие частичных зарядов в отдельных частях молекулы еще не означает образования ионов. Ковалентная связь, при образовании которой электронная пара смещается в сторону одного из атомов, называется полярной связью.
В соединениях элементов одного периода общая электронная пара смещается в сторону атома того элемента, который в таблице стоит правее. В соединениях элементов одной подгруппы электронная пара смещается в направлении атома элемента с меньшей атомной массой.
Полярные молекулы можно рассматривать как электрические диполи, в которых разные по знаку, но одинаковые по величине заряды расположены на определенном расстоянии друг от друга. Мерой полярности молекул служит дилольный момент, представляющий собой произведение величины заряда на расстояние между центрами положительного и отрицательного зарядов в молекуле. Наличие или отсутствие дипольного момента у молекулы часто позволяет судить о её геометрическом строении. Например, для молекулы типа AB2 возможно линейное или угловое строение:
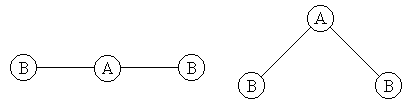
Линейная структура характеризуется симметричным распределением зарядов и отвечает неполярной молекуле. Напротив, в молекуле, имеющей угловое строение, заряды распределяются асимметрично. Такая молекула полярна. Из того факта, что молекула CO2 неполярна, а мслекула SO2 обладает дипольным моментом, можно сделать вывод о линейном строении молекулы диоксида углерода и угловом строении молекулы диоксида серы.
Зависимость между полярностью молекулы и полярностью связей между атомами в этой молекуле не однозначна. Так, отсутствие в молекуле полярных свявей обусловливает и неполярность самой молекулы. Напротив, наличие в молекуле полярных связей еще не означает полярности молекулы. Например, линейная молекула диоксида углерода O=C=O и треугольная молекула трифторида бора BF3 неполярны, хотя имеют полярные связи. Неполярность этих молекул объясняется совпадением центров тяжести положительных и отрицательных зарядов в них вследствие симметричности расположения связей в молекулах. В большинстве случаев неполярными являются также молекулы, содержащие гибридизованные связи тила sp, sp2, sp3, sp3d2. Молекулы, связи в которых образованы двумя или тремя чистыми p-орбиталями (например, H2S, AsCl3), полярны.
Полярность молекул в значительной мере определяет свойства веществ. Полярные молекулы поворачиваются друг к другу разноимённо заряженными полюсами, и между ними возникает взаимное притяжение. Поэтому вещества, образованные полярными молекулами, имеют более высокие температуры плавления и кипения, чем вещества, молекулы которых неполярны.
Жидкости, молекулы которых полярны, имеют более высокую растворяющую способность. При этом чем больше полярность молекул растворителя, тем выше растворимость в ней полярных или ионных соединений. Эта зависимость объясняется тем, что полярные молекулы растворителя за счет диполь-дипольного или ион-дипольного взаимодействия с растворяемым веществом способствуют распаду растворяемого вещества на ионы. Например, раствор хлороводорода в воде, молекулы которой полярны, хорошо проводит электрический ток. Раствор хлороводорода в бензоле не обладает заметной электропроводностью. Это указывает на отсутствие ионизации хлороводорода в бензольном растворе, так как молекулы бензола неполярны.
Количественную характеристику полярности связи можно получить, сопоставляя значения электроотрицательности элементов. Эта величина представляет собой арифметическую сумму энергии ионизации и сродства к электрону. За единицу принята электроотрицательность лития. Электроотрицательность других элементов выражается в относительных величинах и равна 0,9 для натрия, 0,8 для калия, 2,1 для водорода, 3 для азота, 3,5 для кислорода, 3 для хлора, 4 для фтора, 2,5 для углерода и т. д.
Смотрите также
РН-метрия
Потенциометрическое
титрование широко используется в лабораторной практике. Оно применяется в тех случаях,
когда надо провести экспресс-анализ вещества, а необходимых реактивов и
оборудован ...
Физико-химические методы исследования бетонных образцов
С
28 июня по 24 июля 2010 года я проходил практику в Дальневосточном научно - исследовательском
институте строительных материалов Российской академии архитектуры и
строительства Центре &quo ...
Тонкослойная хроматография и ее роль в контроле качества пищевых продуктов
Хроматография,
обязательно включающая процесс разделения смесей веществ в динамическом режиме,
охватывает не только достаточно обширный раздел аналитической химии, но и лежит
в основе ряда ...


