Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Валентность атома углерода в
органических соединенияхДипломы, курсовые и прочее / Органическая химия / Дипломы, курсовые и прочее / Органическая химия / Валентность атома углерода в
органических соединениях Валентность атома углерода в
органических соединениях
Атомы углерода, входящие в состав органических соединений, всегда будут четырёхвалентны, имеют электронную конфигурацию 1s2s22p2 и могут находиться в трех валентных состояниях
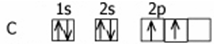
Первое валентное состояние (на примере метана СН4). При образовании молекулы метана атом углерода переходит в возбужденное состояние:
![]()
Четыре неспаренных электрона (2s и 2р) участвуют в образовании четырех б - связей. При этом возникают гибридные орбитали. Гибридизация орбиталей - процесс выравнивания их по форме и энергии. Число гибридных орбиталей равно числу исходных орбиталей. В молекуле метана и во всех молекулах органических веществ по месту одинарной связи атомы углерода будут находиться в состоянии бр3 - гибридизации, т.е. у атома углерода гибридизации подверглись орбитали одного s - и трех р - электронов и образовались 4 одинаковые гибридные орбитали.
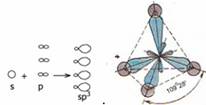
sp3 – гибридные облака располагаются под углом 109°28`.
Второе валентное состояние атома углерода на примере этилена (C2H4)
В молекуле этилена каждый атом углерода соеденён с тремя другими атомами, поэтому в гибридизацию вступают З орбитали: одна s и две р, т.е. происходит sр2 - гибридизация.
Эти орбитали располагаются под углом 120° по отношению друг к другу.
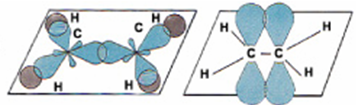
Две негибридные орбитали перекрываются перпендикулярно плоскости и образуют – связь.
Третье валентное состояние атома углерода (на примере ацетилена С2Н2). В молекуле ацетилена атом углерода соединен с двумя другими атомами, поэтому в гибридизацию вступают две орбитали: одна s и одна p, т.е. происходит sp-гибридизация.
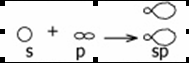
Эти орбитали располагаются под углом 180º по отношению друг к другу.

Не вступившие в гибридизацию две p-отбитали при боковом перекрывании образуют две π-связи, расположенные во взаимно перпендикулярных плоскостях.

Смотрите также
Обзор литературы
По своему
химическому составу вода является соединением двух атомов водорода и одного
атома кислорода. Однако, в естественных условиях в воде постоянно содержаться
самые различные вещества и элемен ...
Комплексные соединения в аналитической химии
Обширную группу
химических соединений составляют комплексы, в молекулах которых всегда можно
выделить центральный атом или ион, вокруг которого сгруппированы другие ионы
или молекулярные гр ...
Ознакомление с некоторыми операциями
лабораторной практики и измерительными приборами.
Цель
работы - ознакомление студентов с взвешиванием, измерением объемов жидкостей,
титрованием и др., а также с некоторыми химическими и измерительными приборами.
При подготовке к
выполнению ла ...


