Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Строение атома углерода (С),
структура его электронной оболочки. Значение атома углерода (С) в химическом строении
органических соединенийДипломы, курсовые и прочее / Органическая химия / Дипломы, курсовые и прочее / Органическая химия / Строение атома углерода (С),
структура его электронной оболочки. Значение атома углерода (С) в химическом строении
органических соединений Строение атома углерода (С),
структура его электронной оболочки. Значение атома углерода (С) в химическом строении
органических соединенийСтраница 1
УГЛЕРОД (лат. Carboneum), С, химический элемент подгруппы IVa периодической системы; атомный номер 6, атомная масса 12,0107, относится к неметаллам. Природный углерод состоит из двух стабильных нук лидов - 12С (98,892% по массе) и 13С (1,108%) и одного нестабильного - С с периодом полураспада 5730 лет.
Распространённость в природе. На долю углерода приходится 0,48% от массы земной коры, в которой он по содержанию занимает среди других элементов 17-е место. Основные углерод-содержащие породы - природные карбонаты (известняки и доломиты); количество углерода в них составляет около 9,610 т.
В свободном состоянии углерод встречается в природе в виде горючих ископаемых, а также в виде минералов - алмаза и графита. Около 1013 т углерода сосредоточено в таких горючих ископаемых, как каменный и бурый уголь, торф, сланцы, битумы, образующих мощные скопления в недрах Земли, а также в природных горючих газах. Алмазы чрезвычайно редки. Даже алмазоносные породы (кимберлиты) содержат не более 9-10 % алмазов массой, как правило, не более 0,4 г. Найденным крупным алмазам обычно присваивают особое название. Самый большой алмаз «Куллинан» весом 621,2 г (3106 карат) был найден в Южной Африке (Трансвааль) в 1905 г., а самый большой русский алмаз «Орлов» весом 37,92 г (190 карат) -в Сибири в середине 17 в.
Чёрно-серый непрозрачный жирный на ощупь с металлическим блеском графит представляет собой скопление плоских полимерных молекул из атомов углерода, непрочно наслоённых друг на друга. При этом атомы внутри слоя связаны между собой сильнее, чем атомы между слоями.
Другое дело алмаз. В его бесцветном, прозрачном и сильно преломляющем свет кристалле каждый атом углерода связан химическими связями с четырьмя такими же атомами, расположенными в вершинах тетраэдра. Все связи одинаковы по длине и очень прочны. Они образуют в пространстве непрерывный трёхмерный каркас. Весь кристалл алмаза представляет собой как бы одну гигантскую полимерную молекулу, не имеющую «слабых» мест, т.к. прочность всех связей одинакова.
Плотность алмаза при 20°С равна 3,51 г/см3, графита - 2,26 г/см3. Физические свойства алмаза (твёрдость, электропроводность, коэффициент термического расширения) практически одинаковы по всем направлениям; он является самым твёрдым из всех найденных в природе веществ. В графите же эти свойства по разным направлениям - перпендикулярному или параллельному слоям атомов углерода - сильно различаются: при небольших боковых усилиях параллельные слои графита сдвигаются друг относительно друга и он расслаивается на отдельные чешуйки, оставляющие след на бумаге. По электрическим свойствам алмаз - диэлектрик, графит же проводит электрический ток.
Алмаз при нагревании без доступа воздуха выше 1000 °С превращается в графит. Графит при постоянном нагревании в тех же условиях не изменяется вплоть до 3000°С, когда он возгоняется без плавления. Прямой переход графита в алмаз происходит только при температуре выше 3000°С и огромном давлении - около 12 ГПа.
Третья аллотропная модификация углерода -карбин - получена искусственно. Это мелкокристаллический чёрный порошок; в его структуре длинные цепочки атомов углерода расположены параллельно друг другу. Каждая цепочка имеет строение (-С=С)Л или (=С=С=)Л. Плотность карбина средняя между графитом и алмазом -2,68-3,30 г/см3. Одна из важнейших особенностей карбина - его совместимость с тканями человеческого организма, что позволяет применять его, например, при изготовлении не-отторгаемых организмом искусственных кровеносных сосудов (рис. 1).
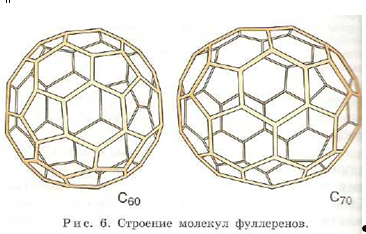
Рис. 1
Название своё фуллерены получили не в честь химика, а по имени американского архитектора Р. Фуллера, который предложил строить ангары и другие сооружения в виде куполов, поверхность которых образуют пяти- и шестиугольники (такой купол построен, например, московском парке «Сокольники»).
Смотрите также
Новейшие достижения современной химии
Химия
постоянно развивается как наука. И не только в теоретическом аспекте. На
нынешнем уровне развития человечества химические открытия приобрели огромное
практическое значение в самых раз ...
Глюкоза
...


