Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Идентификация кинетических параметров процессов растворенияДипломы, курсовые и прочее / Растворение твердых веществ / Дипломы, курсовые и прочее / Растворение твердых веществ / Идентификация кинетических параметров процессов растворения Идентификация кинетических параметров процессов растворения
Если бы найденные нами из экспериментальных исследований константы (константы скорости, порядки реакций и т.д.) использовались для расчета реакторов того же масштаба, что и экспериментальный, то задачу по определению констант можно было бы считать выполненой. Но масштабы промышленных и лабораторных реакторов-растворителей различаються на несколько порядков. Поэтому из экспериментально определенных кажущихся констант и порядков необходимо извлечь то, что характеризует саму химическую реакцию и не зависит от размеров реактора и его элементов. Такое экспериментально-теоретическое исследование называют идентификацией – опознаваемым параметров уравнения кинетики. При идентификации параметров уравнения кинетики гетерогенного процесса необходимо исходить из представлений о лимитирующей стадии процесса.
Признаки, по которым различают в какой области кинетики лежит процесс растворения, представлены в таблице 1.
Таблица 1
Основные признаки различных областей кинетики растворения
|
Факторы, характеризующие растворение |
Область кинетики | |
|
диффузионная область |
собственно кинетическая | |
|
1.Величина коэффициента скорости растворения k (см/сек) при 250С |
10-2÷10-3 |
10-6÷10-7 |
|
2.Температурный коэффициент скорости растворения, kt+10/kt |
≤ 1,5 |
≥ 2 |
|
3.Величина энергии активации растворения Е[кДж/моль] |
≤ 20 |
≥ 40 |
|
4.Зависимость скорости процесса от интенсивности перемешивания раствора |
зависит |
зависит |
|
5.Влияние вязкости раствора на скорость растворения |
влияет |
не влияет |
Ответ о типе кинетики растворения взвешенных кристаллов солей дает уравнение А.Б. Здановского, выведенное из теории подобия и аналитическим путем:
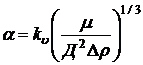 ,
,
где kυ – коэффициент скорости растворения при объемном выражении концентраций (см/сек);
μ – динамическая вязкость пограничного раствора, (г/см·сек);
Д – коэффициент диффузии, (см2/сек);
Δr – разность плотностей кристалла и растворителя (г/см3).
Если α = 15±2, то имеет место диффузионная кинетика растворения.
Если α < 1, то мы имеем дело с кинетической областью.
Если a = 13 ¸ 1, то растворение протекает в переходной области.
Следует также помнить, что подавляющее процессов химического растворения веществ описываются уравнением реакции первого порядка.
Смотрите также
Расчет и проектирование выпарной установки непрерывного действия для выпаривания водного раствора CuSO4
Выпаривание –
процесс концентрирования растворов нелетучих веществ путем удаления жидкого
летучего растворителя в виде паров. Сущность выпаривания заключается в переводе
растворителя в паро ...
Принципы определения примесей арсена в неизвестном минерале
В условиях активного загрязнения окружающей
среды и реальности экологического кризиса возрастает значение научных
исследований, направленных на изучение состояния экосистемы, и практического ...
Исследование концентрирования Cu (II) на анионите АВ-17, иммобилизованном 8-оксихинолином
Количественное определение следовых тяжелых металлов в объектах окружающей среды (природных и сточных водах и т.п.) вызывает у экологов, химиков-аналитиков
определенные затруднения. Это объяс ...


