Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Экспериментальное определение кинетических характеристик. Определение энергии активацииДипломы, курсовые и прочее / Растворение твердых веществ / Дипломы, курсовые и прочее / Растворение твердых веществ / Экспериментальное определение кинетических характеристик. Определение энергии активации Экспериментальное определение кинетических характеристик. Определение энергии активации
При проведении кинетических исследований следует убедиться в безградиентности процесса: повышение интенсивности перемешивания не приводит к росту константы скорости реакции.
Для определения энергии активации необходимо провести не менее двух периодических опытов при различных температурах. В каждом из опытов при фиксированных температурах ![]() и
и ![]() (
(![]() должно быть не менее 100 С для уменьшения погрешности в численном значении энергии активации Е) определяют зависимость доли нерастворившегося компонента от продолжительности растворения:
должно быть не менее 100 С для уменьшения погрешности в численном значении энергии активации Е) определяют зависимость доли нерастворившегося компонента от продолжительности растворения: ![]() и
и ![]() ,
, ![]() (
(![]() - степень растворения вещества). При этом время растворения вещества
- степень растворения вещества). При этом время растворения вещества ![]() и концентрация растворителя во всех опытах должно быть одинаковым или необходимо фиксировать время достижения одинаковых степеней растворения вещества, а все остальные параметры системы должны остаться неизменными.
и концентрация растворителя во всех опытах должно быть одинаковым или необходимо фиксировать время достижения одинаковых степеней растворения вещества, а все остальные параметры системы должны остаться неизменными.
Кинетические функции растворения могут быть представлены в виде:
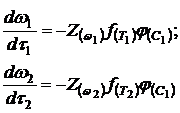 (12)
(12)
Если сравнить скорость растворения при равных значениях ![]() , то
, то ![]() и
и ![]() (т.к. начальные концентрации одинаковы исходя из начально заданных условий, а изменение концентрации в ходе растворения стехиометрически связано с долей растворившегося продукта). Поэтому для равных значений
(т.к. начальные концентрации одинаковы исходя из начально заданных условий, а изменение концентрации в ходе растворения стехиометрически связано с долей растворившегося продукта). Поэтому для равных значений ![]() можно записать:
можно записать:
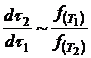 (13)
(13)
Отношение, стоящее в правой части уравнения (13), не зависит от времени.
Интегрируя это уравнение и подставляя вместо ![]() и
и ![]() их значения, равные
их значения, равные ![]() и
и ![]() , получим окончательно:
, получим окончательно:
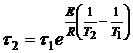 (14)
(14)
Необходимо подчеркнуть, что ![]() и
и ![]() означают время, необходимое для достижения одного и того же значения
означают время, необходимое для достижения одного и того же значения ![]() в первом и втором опытах.
в первом и втором опытах.
Уравнение (14) показывает, что зависимость ![]() от
от ![]() выражается аппроксимирующей линией, тангенс угла наклона которой к оси абсцисс численно равен энергии активации Е/R.
выражается аппроксимирующей линией, тангенс угла наклона которой к оси абсцисс численно равен энергии активации Е/R.
Вместо определения углового коэффициента прямой, энергию активации можно вычислить по формуле:
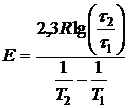 (15)
(15)
Вычисления по формуле (15) в других интервалах ![]() дадут набор значений Е, из которого легко получить наиболее достоверное (среднее) значение энергии активации и среднюю ошибку её определения, которая не должна быть более 10%. В противном случае необходимо искать ошибку в постановке эксперимента или в расчетах. Возможно также изменение механизма процесса растворения. В последнем случае необходимо сузить температурные интервалы и увеличить количество экспериментов.
дадут набор значений Е, из которого легко получить наиболее достоверное (среднее) значение энергии активации и среднюю ошибку её определения, которая не должна быть более 10%. В противном случае необходимо искать ошибку в постановке эксперимента или в расчетах. Возможно также изменение механизма процесса растворения. В последнем случае необходимо сузить температурные интервалы и увеличить количество экспериментов.
Смотрите также
Физиологическое значение висмута
Не смотря на то, что висмут относится к категории
тяжелых металлов, он является умеренно токсичным элементом. Некоторые источники
даже называют висмут "самым безобидным" тяжелым металлом. ...


