Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Метод гетерофункциональной поликонденсацииДипломы, курсовые и прочее / Синтез и исследование поливольфрамофенилсилоксанов, содержащих атомы вольфрама в степени окисления +6 / Дипломы, курсовые и прочее / Синтез и исследование поливольфрамофенилсилоксанов, содержащих атомы вольфрама в степени окисления +6 / Метод гетерофункциональной поликонденсации Метод гетерофункциональной поликонденсацииСтраница 2
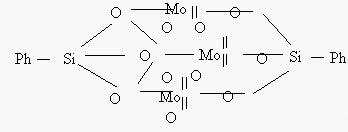
На основе экспериментальных данных было установлено, что наиболее отчетливо перегруппировка наблюдается в случае, когда в структуре силоксановой цепи находится атом переходного металла [22].
Показано, что движущей силой перегруппировки является координационная ненасыщенность металла, находящегося в структуре силоксановой цепи. Предложена схема, объясняющая протекание перегруппировки, включающая стадию образования координационного переходного комплекса.
Рассмотрены экстремальные варианты перегруппировки, находящиеся в полном соответствии с предложенной схемой:
а) глубокое протекание перегруппировки, приводящие к выведению металла в форме оксида из силоксановой матрицы;
б) торможение этого процесса в случаях, когда достижимо заполнение координационной сферы металла за счет "внутренних ресурсов". Показано, что наиболее эффективное торможение перегруппировки достигается при заполнении координационной сферы металла атомами кислорода, входящими в состав группировки Si-O-M, а также силанолят-анионами Si-O-.
Проведен сравнительный анализ состава природных металлосиликатов, в результате которого установлено, что закономерности, выведенные при изучении химии МОС, могут быть приложены к описанию некоторых геохимических процессов образования минералов.
Авторами [23] была предпринята попытка синтеза поливольфрамофенилсилоксанов, содержащих металл в высшей степени окисления, взаимодействием оксихлорида вольфрама (W+6) с полифенилсиликонатом натрия. В результате получен поливольфрамофенилсилоксан с соотношением кремния к металлу равным 14. Резкое отличие соотношения кремния к металлу от заданного в растворимых в органических растворителях продуктах реакции авторы объясняют тем, что окончательное формирование полимерной структуры происходит при температуре кипения растворителей. Учитывая высокую функциональность мономера, это может приводить к образованию сшитых структур, что подтверждается образованием нерастворимых гетеросилоксанов с высоким содержанием металла.
Смотрите также
Новейшие достижения современной химии
Химия
постоянно развивается как наука. И не только в теоретическом аспекте. На
нынешнем уровне развития человечества химические открытия приобрели огромное
практическое значение в самых раз ...
Белки и аминокислоты
Белки – это биологические полимеры, состоящие из аминокислот. Ни один из существующих живых организмов – от вирусов до растений и животных – не может существовать без белка. Правда, ...


