Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Классификация электродовДипломы, курсовые и прочее / Равновесные и поляризационные диаграммы потенциал-pH / Дипломы, курсовые и прочее / Равновесные и поляризационные диаграммы потенциал-pH / Классификация электродов Классификация электродовСтраница 2
Ртутно-оксидный электрод: Hg2O+2e-+H2O=2Hg+2OH-
![]() (1.2.8)
(1.2.8)
Во всех системах, отвечающих электродам 1 и 2-ого, одним из компонентов восстановленной формы служит металл электрода. Если же инертный металл электрода не участвует в полуреакциях, а является только передатчиком электронов между Ox и Red, то такие системы называют окислительно-восстановительными электродами или редокс-системами.
Например, система:
Fe3++e-=Fe2+, 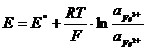
Cu2++e-=Cu+, 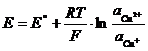
С платиновым электродом в качестве инертного переносчика электронов между Ox и Red.
Среди окислительно-восстановительных электродов выделяют газовые электроды. Газовый электрод состоит инертного металла (часто платины или платинированной платины), к которому подводится электрохимически активный газ. Молекулы газа адсорбируются на поверхности металла, распадаясь при этом на атомы, а адсорбированные атомы участвуют уже непосредственно в электродной реакции. Поскольку между молекулами газовой фазы и адсорбированными атомами устанавливается равновесие, то при записи электродного равновесия промежуточное адсорбционное состояние часто опускают. Примером газового электрода, обратимого по катиону, является водородный электрод, на поверхности которого устанавливается равновесие: H++e-=1/2H2.
Потенциал водородного электрода – это ЭДС цепи:
Pt, H2(p=1)│H3O+(![]() =1) ¦¦ H3O+(
=1) ¦¦ H3O+(![]() )│ H2(p), Pt
)│ H2(p), Pt
Если в правой части цепи положить ![]() =1 и
=1 и ![]() , то цепь окажется полностью симметричной и ее ЭДС должна равняться нулю. Следовательно,
, то цепь окажется полностью симметричной и ее ЭДС должна равняться нулю. Следовательно,
![]() (1.2.9)
(1.2.9)
Смотрите также
Получение метилового эфира монохлоруксусной кислоты
...
Изучение химического состава снега
В эпоху
научно-технической революции антропогенные воздействия на окружающую среду
становятся интенсивными и масштабными. Серьезную опасность представляет
усиливающиеся загрязнение природны ...


