Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Термодинамические функции образования интерметаллидовДипломы, курсовые и прочее / Термодинамика химической устойчивости сплавов системы Mn-Si / Дипломы, курсовые и прочее / Термодинамика химической устойчивости сплавов системы Mn-Si / Термодинамические функции образования интерметаллидов Термодинамические функции образования интерметаллидовСтраница 2
Постоянная Q одинакова для всех сплавов. Постоянная Р зависит от числа р- электронов второго компонента.
Важное значение для количественных расчетов ![]() имеет правильный выбор функции φ. Её вид зависит от площади контакта между атомными ячейками различных компонентов, степени упорядоченности сплава и атомных объемов компонентов. Согласно Миедеме, φ можно аппроксимировать произведением:
имеет правильный выбор функции φ. Её вид зависит от площади контакта между атомными ячейками различных компонентов, степени упорядоченности сплава и атомных объемов компонентов. Согласно Миедеме, φ можно аппроксимировать произведением:
![]() (1.11)
(1.11)
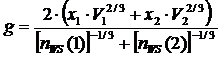 (1.12)
(1.12)
где для MnnSim ![]() ,
, ![]() (1.13)
(1.13)
Для упорядоченной фазы:
![]() (1.14)
(1.14)
![]() - для неупорядоченной фазы первичного твердого раствора.
- для неупорядоченной фазы первичного твердого раствора.
xi – мольные доли, Vi – мольные объемы компонентов сплава, ![]() – «поверхностные» концентрации, определяющие площадь контакта между разнородными атомными ячейками. Их определяют так:
– «поверхностные» концентрации, определяющие площадь контакта между разнородными атомными ячейками. Их определяют так:
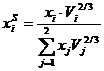 (1.15)
(1.15)
Далее по формуле Истмена рассчитывается энтропия:
![]() (1.16)
(1.16)
Aср. – средняя атомная масса, т. е. молекулярная масса интерметаллида, отнесенная к числу атомов в молекуле соединения, т. е. для сплава MnnSim:
![]() (1.17)
(1.17)
Vср. – средний атомный объем, т. е. средняя атомная масса соединения, отнесенная к его плотности,
![]() (1.18)
(1.18)
![]() (1.19)
(1.19)
Тразл. – температура разложения (плавления), К,
а – константа, равная 52,3 Дж/моль·К
Формулы для расчета ![]() и
и ![]() относятся к 1 г-ат сплава, т.е. величина, относящаяся к 1 молю соединения, делится на число входящих в него атомов. Это удобно для сопоставления термодинамических свойств в различных интерметаллидах [4].
относятся к 1 г-ат сплава, т.е. величина, относящаяся к 1 молю соединения, делится на число входящих в него атомов. Это удобно для сопоставления термодинамических свойств в различных интерметаллидах [4].
Табл. 1.2. Значения постоянных P, Q и R для сплавов переходных металлов [4]
|
Второй компонент интерметаллида |
R |
P |
Q |
|
Переходные металлы (Fe, Co, Ni, Cr, Mn и т. п.) |
0 |
14,2 |
9,4 |
|
Cu, Ag, Au |
0 |
14,2 |
9,4 |
|
Ca, Sr, Ba |
0 |
12,3 |
9,4 |
|
Щелочные металлы |
0 |
12,3 |
9,4 |
|
Be, Mg |
0,4 |
12,3 |
9,4 |
|
Zn, Cd, Hg |
1,4 |
12,3 |
9,4 |
|
B, Al, Ga, In, Tl |
1,9 |
12,3 |
9,4 |
|
C, Si, Ge, Sn, Pb |
2,1 |
12,3 |
9,4 |
|
N, Sb, Bi |
2,3 |
12,3 |
9,4 |
Смотрите также
Характеристика химического элемента №16 (Сера)
...
Гидроксикарбонильные соединения. Дикарбоновые кислоты
a-Гидроксикарбонильные
соединения, как уже отмечалось, могут быть получены окислением диолов
гипобромитом натрия или реагентом Фентона.
Для
a-гидроксикарбонильных
соединений характерна ...
О спонтанном деформировании ацетатных волокон в парах нитрометана
Целлюлоза – один из
наиболее распространенных природных полимеров, широко используемых в различных
областях народного хозяйства. Также широко применяются производные целлюлозы,
особенно аце ...


