Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Расчет диаграммы состояния системы Ni-Si-O при 25 0С.
Анализ химической устойчивостиДипломы, курсовые и прочее / Термодинамика химической и электрохимической устойчивости сплавов системы Ni-Si / Дипломы, курсовые и прочее / Термодинамика химической и электрохимической устойчивости сплавов системы Ni-Si / Расчет диаграммы состояния системы Ni-Si-O при 25 0С.
Анализ химической устойчивости Расчет диаграммы состояния системы Ni-Si-O при 25 0С.
Анализ химической устойчивостиСтраница 1
Как следует из экспериментальных данных по системе никель-кремний (рис.1.1), никель-кислород (рис.1.3) и кремний-кислород (рис.1.4) схема фазовых равновесий в системе никель-кремний-кислород при 298 К и 1 атм. имеет вид (рис.2.2).
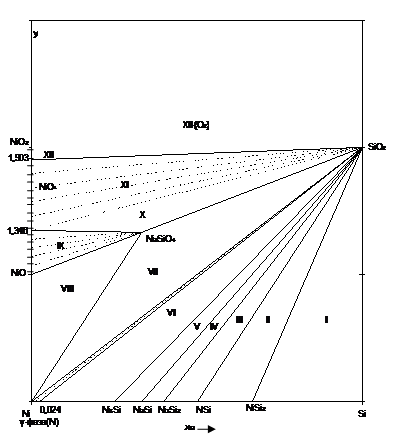
Рис.2.2 Фазовая диаграмма состояния системы Ni-Si-O при 25 0С.
Поскольку химическое сродство кремния к кислороду выше, чем никеля, то можно предположить, что почти при любом составе сплава Ni-Si в первую очередь будет реализовываться равновесие сплав - SiO2.
На диаграмме 2.2 можно выделить области, в которых присутствуют следующие фазы:
1. Si (γ) - NiSi2 - SiO2; (I)
2. NiSi2 - NiSi - SiO2; (II)
3. NiSi - Ni3Si2 - SiO2; (III)
4. Ni3Si2 - Ni2Si - SiO2; (IV)
5. Ni2Si - Ni3Si - SiO2; (V)
6. Ni3Si - γ-фаза - SiO2; (VI)
7. γ - фаза - Ni2SiO4 - NiO; (VII)
8. γ-фаза - Ni2SiO4 - NiO; (VIII)
9. Ni2SiO4 - NiOх, 1<x<1,346; (IX)
10. Ni2SiO4 - SiO2 - NiOx, 1,346<x<1,903; (XI)
Примеры расчета:
а) Фазовое равновесие VII:
γ-фаза - Ni2SiO4 - SiO2 было описано независимыми реакциями образования SiO2 и Ni2SiO4 из компонентов γ-фазы (Ni, Si) и компонентов газовой фазы O2:
(1) ![]() ;
;
(2) ![]() ;
;
![]()
![]()
Константы равновесия реакций 1 и 2:
![]() ; (2.3),
; (2.3), ![]() ; (2.4)
; (2.4)
Для определения состава γ-фазы исключим ![]() из конечного термодинамического уравнения. Для этого возведем уравнение (2.3) в квадрат и поделим полученное на уравнение (2.4), получим:
из конечного термодинамического уравнения. Для этого возведем уравнение (2.3) в квадрат и поделим полученное на уравнение (2.4), получим:
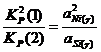 ; (2.5)
; (2.5)
Это уравнение можно переписать в виде:
![]() ; (2.6)
; (2.6)
Из уравнения изотермы химической реакции:
![]() ; (2.7)
; (2.7)
уравнение (2.3.4) можно переписать:
![]() ; (2.8)
; (2.8)
Данное трансцендентное уравнение можно решить только численным методом. Обозначив xSi=x, xNi=x-1, получим:
![]() ; (2.9)
; (2.9)
![]() ; (2.10)
; (2.10)
Подставив уравнения (2.9) и (2.10) в (2.8) решаем численным методом, находим значение х. Исходя из уравнений (2.3) или (2.4) определяем величину ![]() .
.
Для остальных трехфазных равновесий расчет производился тоже исходя из константы равновесия. Например, для равновесия IV:
![]()
Мольные доли компонентов равны единице, поэтому выражение для константы равновесия упрощается:
![]()
![]() ; (2.11)
; (2.11)
Результаты расчетов приведены в таблице 2.5.
Таблица 2.5.
Характеристики фазовых равновесий системы Ni-Si-O при 25 0С
|
№ |
Равновесие |
|
Равновесный состав фаз |
|
I |
Si (γ) - NiSi2 - SiO2 |
1,07*10-156 |
|
|
II |
NiSi2 - NiSi - SiO2 |
3,35*10-150 |
|
|
III |
NiSi - Ni3Si2 - SiO2 |
1,48*10-144 |
|
|
IV |
Ni3Si2 - Ni2Si - SiO2 |
2,00*10-135 |
|
|
V |
Ni2Si - Ni3Si - SiO2 |
1,27*10-128 |
|
|
VI |
Ni3Si - γ-фаза - SiO2 |
3,04*10-129 |
|
|
VII |
γ - фаза - Ni2SiO4 - SiO2 |
2,44*10-81 |
|
|
VIII |
γ - фаза - Ni2SiO4 - NiO |
8,68*10-75 |
|
|
IX |
Ni2SiO4 - NiOх, 1<x<1,346 |
0,21 |
|
|
X |
Ni2SiO4 - SiO2 - NiOx, 1,346<x<1,903 |
0,21 |
|
|
XI |
NiO1,903 - NiO2 - SiO2 |
9,48*1030 |
|
Смотрите также
Белки и аминокислоты
Белки – это биологические полимеры, состоящие из аминокислот. Ни один из существующих живых организмов – от вирусов до растений и животных – не может существовать без белка. Правда, ...
Производство уксусной кислоты
Уксусная кислота — первая из органических кислот, которая стала известна
человеку. Впервые она была получена И.Глаубером в 1648 г. и в концентрированном виде путем вымораживания ее водных рас ...
Получение хлора методом электролиза повареной соли
Быстрое
развитие хлорной промышленности связано в основном с расширением производства
хлорорганических продуктов – винилхлоридов, хлорорганических растворителей,
инсектицидов и др. Хотя дол ...


