Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Результаты эксперимента и их обсуждениеДипломы, курсовые и прочее / Поиск оптимального содержания пигмента в покрытиях на основе алкидного лака ПФ-060 / Дипломы, курсовые и прочее / Поиск оптимального содержания пигмента в покрытиях на основе алкидного лака ПФ-060 / Результаты эксперимента и их обсуждение Результаты эксперимента и их обсуждениеСтраница 7
После изготовления грунтовок и формирования покрытий на их основе полученные образцы окрашенной стали были подвергнуты коррозионным испытаниям (500 часов выдержки в 3%-ном водном растворе хлорида натрия).
В качестве функций отклика использовались значения потенциала стали под покрытием, электрической емкости системы окрашенный металл – электролит, адгезии покрытий и площади подпленочной коррозии.
На рисунках 5.4 и 5.5 представлены результаты исследования изменения значения электрической емкости систем окрашенный металл – электролит; на рисунках 5.6 и 5.7 – хронопотенциометрические кривые, полученные в результате исследования окрашенной стали, находящейся в контакте с электролитом.
Значения электрической емкости большинства образцов находятся в пределах значений, характерных для покрытий с высокими барьерными свойствами – до 2,5 нФ, исключение составляют 1, 2 и 9 композиции, значения емкости для которых увеличиваются, что свидетельствует о снижении барьерных свойств этих образцов и возможном развитии коррозионных процессов.
Анализ результатов хронопотенциометрии стали с покрытиями на основе алкидного связующего показывает наличие хороших защитных свойств у составов 1, 3, 4, 5, 6, 8, коррозионный потенциал которых находится в области положительных значений, что свидетельствует о пассивном состоянии металла под покрытием. Хронопотенциометрические кривые остальных образцов лежат в области отрицательных значений потенциала, что характеризует протекание коррозионных процессов на границе металл – покрытие.
Полную характеристику всем составам можно дать только после проведения комплексной оценки металла и покрытия после окончания испытаний, результаты которой приведены в таблице 5.8.
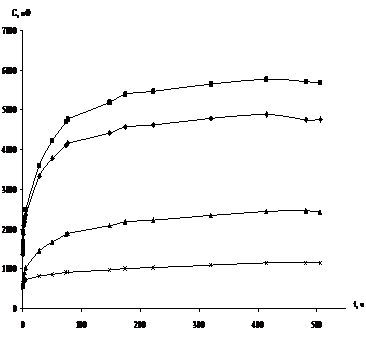
1 – состав 1
2 – состав 2
3 – состав 3
4 – состав 4
Рисунок 5.4 – Изменение значений электрической емкости системы электролит - окрашенный металл

1 – состав 5
2 – состав 6
3 – состав 7
4 – состав 8
5 – состав 9
Рисунок 5.5 – Изменение значений электрической емкости системы электролит – окрашенный металл

1 – состав 1
2 – состав 2
3 – состав 3
4 – состав 4
Рисунок 5.6 - Изменение значений коррозионного потенциала системы электролит – окрашенный металл

1 – состав 5
2 – состав 6
3 – состав 7
4 – состав 8
5 – состав 9
Рисунок 5.7 – Изменение значений коррозионного потенциала системы электролит – окрашенный металл
Таблица 5.8 – Результаты комплексной оценки состояния образцов стали с пигментированными покрытиями, содержащими манганат (IV) силикат кальция
|
№ состава |
С, нФ |
Е, мВ |
Пузыри,% |
Площадь коррозии, % |
Адгезия, баллы | |
|
до опыта |
после опыта | |||||
|
1 |
4,76 |
110 |
3 |
5 |
1 |
1 |
|
2 |
5,68 |
-54 |
7 |
3 | ||
|
3 |
2,23 |
185 |
0 |
0 | ||
|
4 |
1,15 |
90 |
0 |
0 | ||
|
5 |
2,39 |
8 |
10 |
5 | ||
|
6 |
1,17 |
60 |
0 |
0 | ||
|
7 |
2,24 |
-251 |
20 |
7 | ||
|
8 |
0,80 |
136 |
0 |
0 | ||
|
9 |
4,53 |
-110 |
10 |
3 | ||
Смотрите также
Исследование механизма электровосстановления ионов самария в
хлоридных и хлоридно - фторидных расплавах.
Исследование процесса
электровосстановления ионов Sm3+ вольтамперометрическим методом при
стационарных и нестационарных режимах поляризации проводилось в трехэлектродной
ячейке. В качестве индикат ...
Получение и изучение сульфатов микрокристаллической целлюлозы древесины осины
Сложные эфиры
целлюлозы имеют широкое применение для производства, этим объяснятся большое
количество работ посвященных всестороннему изучению эфиров целлюлозы.
Сернокислые эфиры
(сульфа ...
Сорбируемость меди на бурых углях, сапропелях и выделенных из них гуминовых кислотах
Проблема очистки воды для хозяйственно - питьевых нужд от
токсикантов, в частности, от соединений тяжелых металлов, является весьма
актуальной природоохранной проблемой в Тульском регионе, в ...


