Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Атомарный хлорДипломы, курсовые и прочее / Роль свободных радикалов в природной среде / Дипломы, курсовые и прочее / Роль свободных радикалов в природной среде / Атомарный хлор Атомарный хлорСтраница 1
Главный источник атомарного хлора – антропогенный. Атомарных хлор образуется в результате фотохимического разрушения фреонов (фторхлорметанов или ФХУ), применяющихся в качестве хладоагентов (их др.название хладоны) в холодильных установках, кондиционерах и в качестве пропеллентов (средств для образования аэрозолей) в аэрозольных баллончиках, пенных огнетушителях.
Наиболее широко распространенными фреонами является CF2Cl2 (фреон 12) и CFCl3 (фреон 11). (применительно к производству фреон 12 составляет 85% всей мировой продукции F-содержащих соединений)
В молекулы некоторых фреонов так же включен Br наряду с ат. Cl или вместо него – эти вещества называются галлоны (вместо фреонов), например CF2ClBr – гало 1211, CF3Br – галлон 1301
Фреоны химически инертны и очень устойчивы с нижних слоях атмосферы время их жизни в тропосферы ~ 80 лет, таким образом постепенно они (как и N2O) м.б. перенесены в стратосферу.
В стратосфере ( в средних слоях) ХФУ фотохимических разлатапется под действием света с l<214 нм.
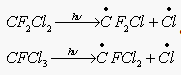
Наряду с фреонами (антропогенного происхождения) в стратосферу спосолен проникать и давать ат Cl природных Cl-содержащий компонент CH3Cl – он выделяется в больших количествах из морской воды, при вулканической дятельности, при горении биомассы ( в результате рекомбинации ![]() )
)
Потенциальная роль отдельных частиц, участвующих разрушении озона, видна из сравнения значений констант скоростей их реакций с озоном (при одной температуре)
|
K, см3/молекул×с | |
|
|
8×10-12 |
|
|
6,7×10-14 |
|
|
2,5×10-15 |
|
|
5×10-16 |
Таким образом наиболее активен в этом процессе ат Cl – его константа скорости на 2-3 порядка выше константы скорости других катализаторов.
Систематические наблюдения, проводимые с середины 70-х годов, указывают на существенное изменение в озоновом слое – снижение концентрации озорна. Учитывая отмеченные факты в качестве гл причины рассматривают поступление в стратосферу фреонов.
Образующиеся при фотолизе фреонов атом Cl имеет "сток" из стратосферы (процесс удаления) по реакции с CH4:
![]()
Исследования отмечают увеличение концентрации HCl в стратосфере, что свидетельствует в пользу ведущей роли фреонов в разрушении озона. Реакция Cl с CH4 разрушает "хлорный" цикл, поскольку HCl неактивен по отношению к озону, но он может быть источником активной формы по реакции с гидроксилом:
![]()
Поэтому HCl относят к так называемым "резервуарным" газам. К образованию "резервуарных" газов приводят и реакции ClO – промежуточная компонента хлорного цикла:
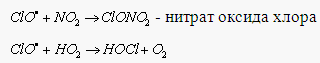
Их фотохимическое разложение генерирует ClO и атомарный хлор – активные к озону частицы.
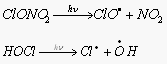
Сходным образом с фреонами ведут себя галлоны – Cl, F, Br, углероды. Они столь же инертны, имеют время жизни в тропосфере примерно 70 лет и могут проникать в стратосферу. Под действием УФ-излучения они разлагаются с выделением Br.
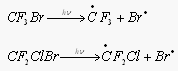
Эти реакции протекают уже в нижней части стратосферы вблизи тропопаузы, таким образом роль атома Br особенно велика в этом слое. Br действует аналогично Cl, разрушая озон в "бромном" цикле, но существенно активнее Cl – один атом Br может разрушить до 100 тыс. молекул озона. Это объясняется малыми скоростями реакции атома Br и BrO, приводящих к неактивным "резервуарным" газам.
Смотрите также
Определение фенола методом броматометрического титрования
...
Бензойная кислота
Систематическое
наименование бензойная кислота
Традиционные
названия бензойная кислота
Химическая
формула C6H5COOH
Молярная масса 122.12
г/моль
Физические
свойства
...
Нестехиометрические твердые оксиды - новые vатериалы современной техники
Обычно об
открытиях в химии сообщается в специальных периодических изданиях - научных и
технических журналах. Немногие из этих сообщений попадают в ежедневные газеты,
потому что массовый чи ...


