Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ПротонированиеДипломы, курсовые и прочее / Электрофильное ароматическое замещение / Дипломы, курсовые и прочее / Электрофильное ароматическое замещение / Протонирование Протонирование
В растворе наблюдается обратимое присоединение протона по всем положениям пиррольного цикла. Наиболее быстро протонируется атом азота, присоединение протона по положению 2 проходит в два раза быстрее, чем по положению 3. В газовой фазе при использовании кислот умеренной силы, таких, как C4H9+ и NH4+, пиррол протонируется исключительно по атомам углерода, причем склонность к присоединению протона по положению 2 выше, чем по положению 3. Наиболее термодинамически стабильный катион - 2Н-пирролиевый ион - образуется при присоединении протона по положению 2 и определяемое значение рКа для пиррола связано именно с этим катионом. Слабая N-основность пиррола обусловлена отсутствием возможности для мезомерной делокализации положительного заряда в 1H-пирролиевом катионе.
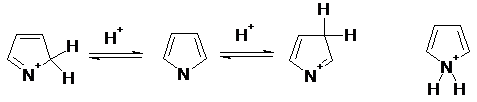
Значение рКа определено для большого числа производных пиррола, а сам незамещенный пиррол — чрезвычайно слабое основание со значением рКа -3,8. Основность пиррольного цикла весьма быстро увеличивается при введении алкильных заместителей, и для 2,3,4,5-тетраметилпиррола рКа равен +3,7, что соответствует полному протонированию всех молекул пиррола в вышеприведенных условиях (для сравнения рКа анилина +4,6). Таким образом, алкильные группы оказывают необычайное стабилизирующее влияние на катионы - пирролы, содержащие трет-бутильные группы, при протонировании образуют стабильные кристаллические соли.
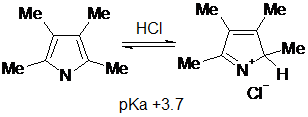
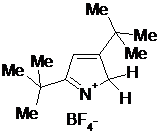
Смотрите также
Химические преобразователи солнечной энергии
Современная энергетика
опирается главным образом на такие источники, в которых запасена солнечная
энергия (СЭ). Прежде всего это ископаемые виды топлива, для образования которых
требуются ...
Получение метилового эфира монохлоруксусной кислоты
...
Алифатические амины
Амины - производные аммиака, в которых атомы водорода замещены на
углеводородные радикалы. Амины классифицируют по числу атомов водорода,
замещенных на углеводородные радикалы. Различают первичные R ...


