Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Кинетические исследованияДипломы, курсовые и прочее / Увеличение степени защиты стали от коррозии в нейтральных и кислых средах / Дипломы, курсовые и прочее / Увеличение степени защиты стали от коррозии в нейтральных и кислых средах / Кинетические исследования Кинетические исследования
С целью определения активационных параметров исследовали кинетику реакции. Кинетическое исследование проводили при соотношении диметилфосфита и борной кислоты 1:3 по количеству выделившегося метанола. Кинетические кривые представлены на рис.6.1. Порядок реакции определяли графическим методом (рис.6.2.). Установлено, что взаимодействие диметилфосфита и борной кислоты протекает в соответствии с кинетическим уравнением второго порядка, на основании которого рассчитаны константы скорости реакции.
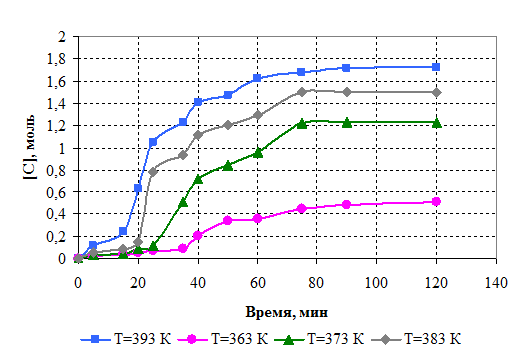
Рисунок 6.1 –
Зависимость выхода метанола от продолжительности реакции.
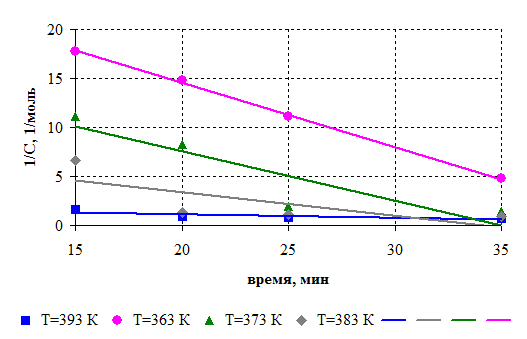
Рисунок 6.2 –
Зависимость обратной величины количества реакционного метанола от времени.
Условия синтеза: борная кислота : диметилфосфит =1:3 (моль/моль), [СБК] = 0,93 моль, [Сдмф] = 2,79 моль. Температура: 363 К; 373 К; 383 К; 393 К.
Таким образом, скорость реакции пропорциональна концентрациям борной кислоты и диметилфосфита в первой степени и сопровождается образованием промежуточных комплексов.
Установлено, что кинетическая вязкость и молекулярная масса снижаются с увеличением количества диметилфофита в реакционной массе, что позволяет судить о прохождении реакции олигомеризации.
Поскольку анаморфоза в координатах ln(Кср) – ( 1/Т ) представлена линейной зависимостью, то активационные параметры поликонденсации подчиняются уравнению Аррениуса (рис.6.3).
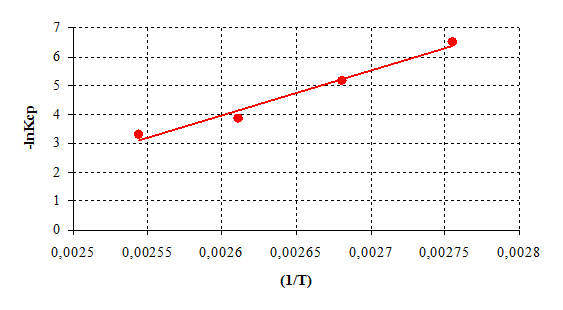
Рисунок 6.3 –
Температурная зависимость скорости реакции борной кислоты с диметилфосфитом
Расчет энергии активации и термодинамических параметров реакции проводили с использованием метода наименьших квадратов. Полученные значения констант средних скоростей реакции сведем в таблицу.
Таблица 6.1 – Активационные параметры реакции
|
Температура, К |
Кср·102, л/моль·с |
Еакт, кДж/моль |
|
363 |
0,1476 |
12,449 |
|
373 |
0,5699 | |
|
383 |
2,1197 | |
|
393 |
3,6655 |
Смотрите также
Тяжелые металлы
Диагноз массового отравления жителей Рима
свинцом поставлен учеными спустя две тысячи лет. Раскопки показали, что древние
римляне пользовались водопроводной системой и посудой из свинца. Сви ...
Правила выживания в химической лаборатории
Если у
вас в руках жидкое - не разлейте, порошкообразное не рассыпьте, газообразное -
не выпустите наружу.
Если
Вы пользуетесь чем-либо - содержите в чистоте и по ...


