Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ПептидыДипломы, курсовые и прочее / Белки и нуклеиновые кислоты / Дипломы, курсовые и прочее / Белки и нуклеиновые кислоты / Пептиды ПептидыСтраница 1
Аминокислоты соединяются друг с другом ковалентной пептидной связью. Образование ее происходит за счет a-аминогруппы (–NH2) одной аминокислоты и a-карбоксильной (–СООН) группы другой с выделением молекулы воды.
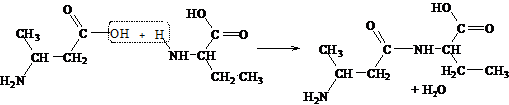
В результате реакции поликонденсации можно получить соединения, составленные из многих аминокислотных остатков – полипептиды. При написании формулы линейных пептидов с известной последовательностью аминокислотных остатков начинают с N-конца (на конце пептида находится свободная a-аминогруппа), используя сокращенные обозначения аминокислот. Названия пептидов складываются из названий соответствующих аминокислот с суффиксом –ил, начиная с N-концевого остатка, – название С-концевой аминокислоты (содержит свободную a-карбоксильную группу) сохраняется. Например, аргинил-аланил-глицин-глутамил-лизин.
Каждый пептид содержит только одну свободную a-амино- и a-карбоксильную группу, которые находятся на концевых остатках аминокислот. Эти группы и R-группы некоторых аминокислот могут быть ионизированы, поэтому пептиды могут нести заряды, и могут быть электронейтральными (т.е. иметь изоэлектрическую точку (ИЭТ). Это свойство пептидов используется для их разделения методами ионной хроматографии и электрофореза. Как и другие соединения, пептиды могут вступать в химические реакции, определяемые наличием у них групп -NH2, -COOH, и R групп-аминокислот. Одной из важных реакций для пептидов является реакция гидролиза. Реакция гидролиза всех пептидных связей путем кипячения растворов пептидов в присутствии сильной кислоты или щелочи используется при определении их аминокислотного состава и состава белков.
Гидролиз пептидных связей может быть осуществлен также действием некоторых ферментов, которые расщепляют пептидные связи избирательно, с образованием коротких пептидов. Например трипсин гидролизует связи образованные карбоксильными группами лизина, аргинина; химотрипсин-карбоксильными группами фенилаланина, тирозина, триптофана. Такой избирательный анализ оказывается очень полезным при установлении аминокислотной последовательности белков и пептидов.
Кроме пептидов, образующихся в результате частичного гидролиза молекул белка, существует много пептидов, встречающихся в живых организмах как свободные соединения.
Многие природные пептиды отличаются по своей структуре от белков; такие пептиды имеются во всех типах организмов. В структурном отношении пептиды небелковой природы весьма разнообразны: отличаются по размерам, наличию циклических структур, разветвленности, наличию D- и a-аминокислот и, в некоторых отдельных случаях, по уникальному строению пептидной связи. Исходя из принципа взаимосвязи структуры и функций, биологические функции таких пептидов также очень многоплановы. Приведем несколько интересных примеров.
Карнозин и Ансерин. Эти дипептиды найдены в мышечных тканях позвоночных, в том числе и в мышцах человека. Оба они содержат b-аланин – структурный изомер a-аланина.
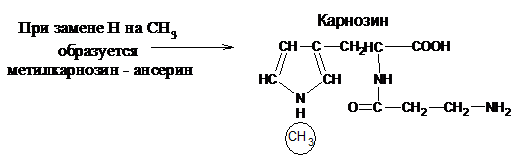
Эти дипептиды служат для поддержания постоянного рН в клетках мышц, т.е действуют как буферы, также они участвуют в сокращении мышц, в процессах окислительного фосфорилирования т.е в образовании АТФ.
Глутатион (g-глутамилцистеинилглицин) – трипептид, присутствует во всех животных, растениях и микроорганизмах.
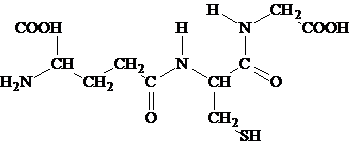
Отличительная структурная особенность глутатиона, состоит в том, что глутаминовая кислота в составе этого пептида представляет для образования пептидной связи g-карбоксильную (а не a-карбоксильную группу). Существуют две формы глутатиона восстановленная (SH-глутатион) и окисленная (S-S-глутатион). Взаимопревращения одной формы в другую катализируется ферментом глутатионредуктазой.

В настоящее время известны лишь некоторые из физиологических функций глутатиона:
Смотрите также
Основные химические законы
Когда впервые
обнаруживается, что некоторая идея объясняет или коррелирует многие факты, то
такую идею называют гипотезой. Гипотезу можно подвергнуть дальнейшей
проверке и экспериментально ...
Нефть и спсобы ее переработки
...
Атом гелия. Двухэлектронный коллектив на примере атома гелия
1. Обозначение электронной конфигурации – это последовательное перечисление АО с указанием числа электронов справа от символа АО.
2. ...


