Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Парциальная константа адсорбционного равновесия при адсорбции
из водных растворов на пористых углеродных сорбентахДипломы, курсовые и прочее / Физико-химические основы адсорбционной очистки воды от органических веществ / Дипломы, курсовые и прочее / Физико-химические основы адсорбционной очистки воды от органических веществ / Парциальная константа адсорбционного равновесия при адсорбции
из водных растворов на пористых углеродных сорбентах Парциальная константа адсорбционного равновесия при адсорбции
из водных растворов на пористых углеродных сорбентах
Парциальную константу адсорбционного равновесия ![]() можно представить следующим уравнением:
можно представить следующим уравнением:
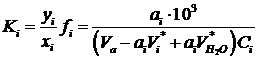 (12)
(12)
где ![]() и
и ![]() – молярные доли растворенного вещества в адсорбционной фазе и равновесном состоянии;
– молярные доли растворенного вещества в адсорбционной фазе и равновесном состоянии; ![]() – удельная адсорбция растворенного вещества;
– удельная адсорбция растворенного вещества; ![]() – предельно-адсорбционный объем пор адсорбента;
– предельно-адсорбционный объем пор адсорбента; ![]() – молярный объем;
– молярный объем; ![]() – парциальный коэффициент активности компонента;
– парциальный коэффициент активности компонента; ![]()
Это – уравнение парциальной изотермы адсорбции, поскольку оно связывает равновесные величины адсорбции данного компонента с его равновесной концентрацией. Необходимые для расчетов величины молярных объемов компонентов раствора могут быть вычислены из их плотности в жидком состоянии:
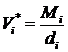 (13)
(13)
где ![]() – плотность жидкого компонента;
– плотность жидкого компонента; ![]() – его молекулярная масса.
– его молекулярная масса.
Эти же величины можно найти как произведение ван-дер-ваальсовской площади проекции адсорбированной молекулы на ван-дер-ваальсовский размер ее, нормальный к плотности проекции ![]() , т.е. на так называемую толщину молекулы.
, т.е. на так называемую толщину молекулы.
В уравнение парциальной изотермы адсорбции удобно вести величину относительного заполнения объема адсорбционной фазы органическим компонентом ![]() . Поскольку
. Поскольку ![]() , а уравнение (13) можно записать в следующем виде:
, а уравнение (13) можно записать в следующем виде:
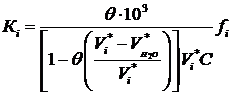 (14)
(14)
При вычислении константы адсорбционного равновесия в качестве стандартного выбрано состояние бесконечного разбавления в растворе в адсорбционной фазе, когда заполнение адсорбционной фазы стремится к нулю.
Поскольку коэффициент активности ![]() в уравнении (14) становится равным единице для стандартного состояния, т.е. при бесконечно малой величине
в уравнении (14) становится равным единице для стандартного состояния, т.е. при бесконечно малой величине ![]() , для нахождения числового значения константы адсорбционного равновесия экспериментальные данные, изображенные в координатах
, для нахождения числового значения константы адсорбционного равновесия экспериментальные данные, изображенные в координатах ![]() , должны быть экстраполированы до значения
, должны быть экстраполированы до значения ![]() . На рис. 5 показано графическое выделение логарифма парциально константы адсорбционного равновесия хлороформа, фенола, анилина, n-хлоранилина, n-нитрофенола, нитробензола и n-нитроанилина из водных растворов на угле КАД (по уравнениям (13) и (14)).
. На рис. 5 показано графическое выделение логарифма парциально константы адсорбционного равновесия хлороформа, фенола, анилина, n-хлоранилина, n-нитрофенола, нитробензола и n-нитроанилина из водных растворов на угле КАД (по уравнениям (13) и (14)).
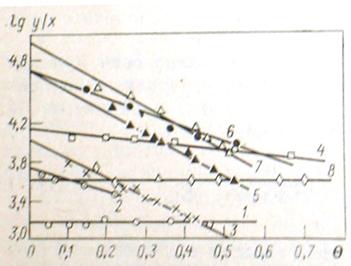
Рис. 5. Графическое вычисление парциальной константы адсорбционного равновесия хлороформа (1), фенола (2), анилина (3), n-хлоранилина (4), n-нитрофенол (5), нитробензол (6) и n-нитроанилин (7) на активном угле КАД и бензола (8) на ацетиленовом техническом углероде (саже)
Из рис. 5 видно, что в подавляющем большинстве случаев существует линейная зависимость между ![]() и
и ![]() , что облегчает экстраполяцию значения
, что облегчает экстраполяцию значения ![]() до
до ![]() . В этом методе используются только определяемые величины: предельно-адсорбционный объем пор адсорбента и молярный объем адсорбируемого вещества, что делает применение метода особенно удобным для практических вычислений.
. В этом методе используются только определяемые величины: предельно-адсорбционный объем пор адсорбента и молярный объем адсорбируемого вещества, что делает применение метода особенно удобным для практических вычислений.
Смотрите также
Электролиз.
Цель работы - ознакомление
с процессами, протекающими на растворимых и нерастворимых электродах при
электролизе водных растворов электролитов.
Электролиз - это
окислительно-восстановительный ...
Расчет ректификационной колонны
...
Введение.
В связи с возрастающим применением РЗМ и
различных материалов на их основе и с добавками редкоземельных металлов в
различных областях науки и техники, в частности, в химической,
металлургической, ...


