Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Сорбция
из водных растворовДипломы, курсовые и прочее / Физико-химические основы адсорбционной очистки воды от органических веществ / Дипломы, курсовые и прочее / Физико-химические основы адсорбционной очистки воды от органических веществ / Сорбция
из водных растворов Сорбция
из водных растворовСтраница 1
Материал, на поверхности пор которого происходит концентрирование поглощаемого вещества, называют адсорбентом, а само вещество — адсорбатом. Адсорбционные явления основаны на физическом и химическом взаимодействии адсорбата и адсорбента.
Силы молекулярного взаимодействия, в основном, дисперсионные, обуславливающие физическую адсорбцию, возникают при сближении молекул материала адсорбента и адсорбируемого вещества и проявляются в упорядочении движения частиц вследствие взаимного притяжения. Дисперсионные взаимодействия неспецифичны, присущи всем веществам и различаются в конкретных случаях лишь количественно. Потенциальная энергия взаимодействия двух атомов равна
![]() (1)
(1)
где r — расстояние между центрами атомов; b — эмпирическая константа; Сn — константа поляризации.
Приведенное выражение показывает, что адсорбционные взаимодействия проявляются только на очень малых расстояниях. Теоретически, если взаимное притяжение атомов максимально на расстоянии r0, то при ![]() их взаимодействие ослабевает в 4 — 5 раз. И, наоборот, при
их взаимодействие ослабевает в 4 — 5 раз. И, наоборот, при ![]() превалируют силы отталкивания. Иногда дисперсионные взаимодействия усиливаются водородными связями и электростатическими (индукционными или ориентационными) силами. Эти дополнительные взаимодействия специфичны для определенного вида адсорбируемых веществ или свойств поверхности адсорбента. Адсорбция – процесс самопроизвольный, протекающий с выделением некоторого количества теплоты,
превалируют силы отталкивания. Иногда дисперсионные взаимодействия усиливаются водородными связями и электростатическими (индукционными или ориентационными) силами. Эти дополнительные взаимодействия специфичны для определенного вида адсорбируемых веществ или свойств поверхности адсорбента. Адсорбция – процесс самопроизвольный, протекающий с выделением некоторого количества теплоты,
В отличие от физической адсорбции, носящей обратимый характер с сохранением индивидуальности адсорбата и адсорбента, хемосорбция — скорее химический процесс на границе раздела фаз. Этот процесс обычно необратимый и значительно более экзотермичный, чем физическая сорбция.
Сорбция из жидких растворов значительно сложнее, чем из парогазовой смеси, так как включает взаимодействия сорбента с сорбируемым веществом и с растворителем (водой); при этом также следует учитывать взаимодействие растворителя с сорбатом. Поэтому, несмотря на то, что сорбция из водных растворов исследуется и используется почти 200 лет, она изучена значительно менее сорбции из парогазовой фазы. В основном механизм сорбции из растворов в том или ином виде объясняют представлениями, выведенными для газовой фазы, лишь дополняя или ограничивая условиями, специфическими для жидкой фазы. Отличия в подходе к подобному переносу отражаются на виде и точности моделей и расчетов систем сорбционной очистки воды.
Теория полимолекулярной сорбции, в основе которой лежит представление о многослойной сорбции на поверхности макро- и мезопористого сорбента, была разработана Брунауэром, Эметом и Теллером. Однако в практике наибольшее распространение получили микропористые сорбенты, в чрезвычайно малом пространстве микропор которых послойной сорбции вещества на поверхности не происходит. При сорбции в микропорах происходит заполнение части или всего объема их сорбатом, который под действием взаимно усиливающихся и перекрывающихся адсорбционных полей, создаваемых противоположными стенками пор, находится в специфическом уплотненном состоянии. Теории объемного заполнения микропор, разработанная Дубининым и его школой, использует понятие о предельном объеме адсорбционного пространства микропористого сорбента W0. Основное уравнение адсорбции паров и газов на микропористых сорбентах, известное как уравнение Дубинина – Радушкевича, имеет вид:
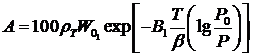 (2)
(2)
При сорбции вещества из раствора оно занимает на поверхности или в объеме пор сорбента место, которое до этого занимали молекулы растворителя (воды), а не свободное пространство. Присутствие воды в порах приводит к некоторому выравниванию сорбционного потенциала. В объеме сорбируемой фазы концентрация вещества значительно выше, чем в растворе. При этом снижается поверхностное натяжение на границе раздела раствор – твердый сорбент.
Смотрите также
Характеристика абсорбционных методов очистки отходящих газов от примесей кислого характера
Грандиозные
масштабы производственной деятельности человека привели к большим позитивным
преобразованиям в мире – созданию мощного промышленного и сельскохозяйственного
потенциала, широкому ...
Технология производства аскорбиновой кислоты (витамина С)
Аскорбиновая кислота впервые выделена
в чистом виде Сцент-Гиорги в 1928 г. под названием гексуроновая кислота. В 1933 г. рядом исследователей установлена ее структура. Синтез ее осуществлен в ...
Реакции спиртов. Кислотно-основные свойства спиртов. Реакции с участием нуклеофильного центра
Спирты представляют собой соединения
общей формулы ROH, в которых гидроксильная группа присоединена к насыщенному
атому углерода. По номенклатуре ИЮПАК насыщенные спирты называют алканолами, ...


