Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Коррозия технических металловУчим химию / Теоретические основы электрохимической коррозии / Учим химию / Теоретические основы электрохимической коррозии / Коррозия технических металлов Коррозия технических металловСтраница 2
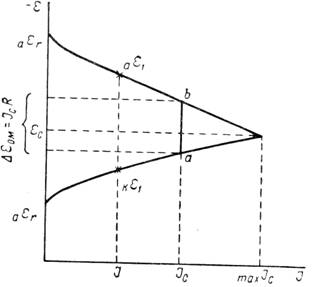
Рисунок 2 - Коррозионная диаграмма
Когда нет коррозионного процесса и сила тока равна нулю, тогда начальные значения потенциалов на аноде и катоде должны отвечать обратимым потенциалам анодной аεr и катодной kεr реакций в заданных условиях. За счет разности потенциалов анода и катода в системе появляется ток. При некоторой силе тока I потенциал анода сместится вследствие поляризации в сторону более положительных, а потенциал катода - в сторону более отрицательных значений. Пусть эти величины будут равны соответственно аε1 и kε1. Разность этих потенциалов под током меньше разности их обратимых потенциалов. С увеличением силы тока разность между потенциалом анода и катода будет непрерывно сокращаться. В пределе она окажется равной нулю, и поверхность корродирующего образца сделается эквипотенциальной. Здесь будет достигнута сила тока, отвечающая максимально возможной в данных условиях скорости коррозии maxIc, а потенциал образца станет равным величине εс , лежащей между аεr и кεr. Это максимальное значение силы тока может быть реализовано лишь тогда, когда сопротивление системы или равно нулю, или ничтожно мало. В противном случае, если омическое падение напряжения не равно нулю, скорость коррозии будет не maxIc , а некоторой меньшей величиной Iс. В этих условиях омическое падение напряжения ∆εOM численно равно длине отрезка ab. Потенциал анода в процессе коррозии будет отрицательнее потенциала катода на величину ∆εOM. Таким образом, скорость коррозии является функцией разности обратимых потенциалов анодной и катодной реакций, их поляризуемости и омического сопротивления коррозионной среды. Влияние каждого из этих факторов на скорость коррозии показано графически на рисунке 3 при помощи упрощенных коррозионных диаграмм. Скорость коррозии уменьшается, если при заданном сопротивлении и неизменной поляризуемости электродов обратимые потенциалы анодной и катодной реакций сближаются (рисунок 3,а), то есть Iс изменяется параллельно с величиной (кεr - аεr). Скорость коррозии становится меньше при увеличении общего сопротивления в системе корродирующий металл - коррозионная среда (рисунок 3,б). Повышение анодной (рисунок 3,в) или катодной (рисунок 3,г) поляризации также уменьшает скорость коррозии. Повышение поляризации может быть результатом появления дополнительных торможений как анодного, так и катодного процессов, либо уменьшением площади анодных или катодных участков. Сокращение площади данного электрода при неизменной силе тока увеличивает на нем плотность тока, а следовательно, и поляризацию.
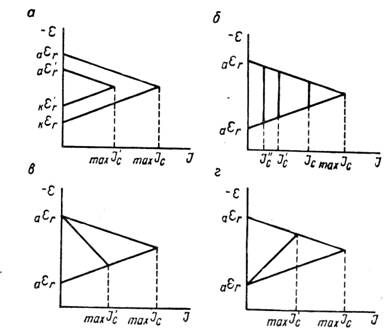
Рисунок 3 - Коррозионные диаграммы влияния различных факторов на скорость коррозии
В теории локальных элементов первоначально предполагалось, что катодный и анодный процессы должны быть обязательно пространственно разделены, и каждый из них может протекать лишь на вполне определенном участке поверхности корродирующего металла. На этом основании считалось, что идеально чистые металлы с совершенно однородной поверхностью не должны подвергаться коррозии. Такое заключение ошибочно и с термодинамической, и с кинетической точек зрения. Чтобы обеспечить протекание коррозии, необходима разница между обратимым потенциалом металла и потенциалами анодной и катодной реакций, возможных в данных условиях, а не пространственное разделение катодных и анодных участков. Анодные и катодные реакции в зависимости от степени однородности границы раздела металл - среда могут протекать на одной и той же поверхности или на ее различных участках. Совмещение катодных и анодных реакций типично для коррозии чистых металлов и амальгам; их более или менее полное пространственное разделение - для коррозии технических металлов. Меньшая стойкость технических металлов по сравнению с чистыми, а также изменение характера коррозионных разрушений во многом связаны с деятельностью гальванических микроэлементов основной металл - включение.
Смотрите также
Автоматизированная система для исследования кинетики быстрых химических реакций
...
Контрольные вопросы.
В чем
состоит главная задача химии?
Основанием
химии является основная двуединая проблема химии. В чем она заключается?
От
каких факторов зависят свойства вещества?
Запишите
четыре концеп ...


