Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Расчёт термодинамических функцийУчим химию / Получение уксусной кислоты / Учим химию / Получение уксусной кислоты / Расчёт термодинамических функций Расчёт термодинамических функцийСтраница 1
Установим зависимость изменения теплоёмкости от температуры Δср= f(T):
Δср=Δa + ΔbT + Δc'T-2 + ΔcT2
Δa=Σ(υa)j – Σ(υa)i = –14,05
Δb= Σ(υb)j – Σ(υb)i = 29,79•10-3
Δc'= Σ(υc')j – Σ(υc')i = 1,88•105
Δc= Σ(υc)j – Σ(υc)i = –15,8•10-6
Стандартные значения изменений термодинамических величин:
ΔН°298 = Σ(υ ΔН°f, 298)j – Σ(υ ΔН°f, 298)i = –218,3 кДж/моль
ΔН°298<0, следовательно реакция экзотермична
ΔS°298 = Σ(υ S°298)j – Σ(S°298)i = –57,77 Дж/моль•К
Согласно уравнению Гиббса-Гельмгольца
ΔG°298 = ΔН°298 – T• ΔS°298 = –201,08 кДж/моль
ΔG°298 <0, следовательно при стандартных условиях реакция может протекать в прямом направлении.
Определим зависимость ΔН°T= f(T), подставив Δср= f(T) в уравнение Кирхгофа:
ΔН°T= ΔН°298 + Δc°pdt = ΔН°298 + Δa(T – 298) + Δb(T2 – 2982)/2 – Δc'(T-1 – 298-1)+ Δc(T3 – 2983)
Подставив в полученную зависимость значения температур в интервале 25 – 175°С, найдём характер изменения зависимости ΔН°f= f(T):
|
Т, К |
313 |
328 |
343 |
358 |
363 |
378 |
393 |
408 |
433 |
448 |
|
–ΔН° Т , кДж/моль |
218,37 |
218,43 |
218,49 |
218,55 |
218,57 |
218,63 |
218,68 |
218,74 |
218,82 |
218,86 |
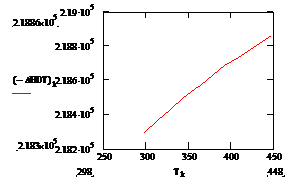
Рис.5 Зависимость теплового эффекта реакции –ΔН°от температуры.
Определим зависимость ΔS°= f(T)
ΔS°T= ΔS°298 + Δc°pdt/T = ΔS°298 + Δa(lnT – ln298) + Δb(T – 298) –
–Δc'/2(T-2 – 298-2)+ + Δc/2(T2 – 2982)
|
Т, К |
313 |
328 |
343 |
358 |
363 |
378 |
393 |
408 |
433 |
448 |
|
–ΔS° Т , Дж/моль |
57,98 |
58,19 |
58,37 |
58,54 |
58,60 |
58,75 |
58,89 |
59,03 |
59,22 |
59,32 |
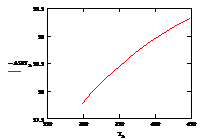
Рис.6 Зависимость изменения энтропии ΔS° от температуры
Пользуясь уравнением Гиббса-Гельмгольца:
ΔG°T = ΔН°T – T • ΔS°T,
рассчитаем значения ΔG° при соответствующих температурах:
|
Т, К |
313 |
328 |
343 |
358 |
363 |
378 |
393 |
408 |
433 |
448 |
|
–ΔG° Т , кДж/моль |
200,22 |
199,35 |
198,47 |
197,59 |
197,30 |
196,42 |
195,54 |
194,65 |
193,18 |
192,29 |
Смотрите также
Жидкофазный металлокомплексный катализ
Все реакционные системы
принято делить на гомофазные и гетерофазные. В первом случае в реакционной
системе отсутствуют границы раздела фаз. Катализатор и реагенты находятся в
одной фазе и в ...
Определение содержания аскорбиновой кислоты в яблоках различных сортов
Большинство зимних сортов яблок отличается невысокой
С-Р витаминностью, и на них можно не останавливаться. Количество витамина С к
весне обычно составляет у яблок половину бывшего к потреби ...
Процессы и аппараты химической технологии
В данной работе стоит задача спроектировать
установку для выпаривания раствора хлорида аммония.
Выпаривание – это
процесс концентрирования растворов твердых нелетучих веществ путем части ...


