Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Методы получения ацетальдегидаУчим химию / Получение уксусной кислоты / Учим химию / Получение уксусной кислоты / Методы получения ацетальдегида Методы получения ацетальдегида
Известен ряд методов получения ацетальдегида. Рассмотрим эти методы.
1.2.1 Получение ацетальдегида гидратацией ацетилена на ртутных катализаторах
Реакция гидратации ацетилена на ртутных катализаторах была открыта М.Г. Кучеровым в 1881 г. и использовалась в промышленности с целью получения ацетальдегида более 60 лет:
![]()
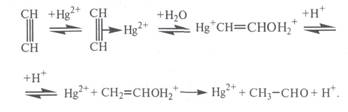
Реакция сильно экзотермична. До 300 °С она практически необратима, но с дальнейшим ростом температуры равновесие смещается в сторону разложения ацетальдегида. Она протекает в нужном направлении с приемлемой скоростью в присутствии катализаторного раствора (10-20%-ная H2SO4, содержащая 0,5-0,6% HgO в виде HgSO4). Реакция протекает через промежуточное образование комплекса ацетилена с Hg2+. Дальнейшее его разложение приводит к образованию ацетальдегида[3, с.440]:
Скорость реакции увеличивается с повышением концентрации H2SO4 и температуры процесса, однако при этом возрастает и выход побочных продуктов, прежде всего за счет кротоновой конденсации с образованием кротонового альдегида: и альдольной конденсации с образованием смол (в том числе и с последующей полимеризацией кротонового альдегида).
![]()
С целью сокращения образования побочных продуктов в реакционную зону подается избыток ацетилена, с которым получающийся ацетальдегид уносится из зоны реакции. Это приводит и к увеличению производительности установки. Вместе с тем подача в избытке ацетилена приводит к уменьшению выхода ацетальдегида за один проход через катализаторный раствор и увеличению рециркуляционных потоков. Конверсия ацетилена в ацетальдегид за один проход составляет 30-50 %.
Ацетальдегид является сильным восстановителем. В данном случае в его присутствии Hg2+ вначале восстанавливается до Hg+, а затем до металлической ртути:
![]()
в результате образуется ртутный шлам. Восстановителями также могут выступать H2S, РН3 и др. Этот процесс является крайне нежелательным, поскольку металлическая ртуть имеет высокое давление насыщенных паров, которые уносятся с реакционными газами, дезактивируя катализатор и загрязняя окружающую среду. Для предотвращения восстановления ртути в катализаторный раствор добавляют соли трехвалентного железа (в избытке по сравнению с солями ртути). Этим обеспечивается протекание реакции
Fe3+ + Hg+ ![]() Fe2+ + Hg2+
Fe2+ + Hg2+
поддерживающей ртуть в максимальной степени окисления.
Соль железа добавляют в избытке по отношению к ртути (~4%: в расчете на Fe2O3), поэтому катализаторный раствор работает достаточно длительное время. Однако в нем постепенно накапливаются соли двухвалентного железа, и раствор направляют на регенерацию, состоящую в окислении азотной кислотой. Несмотря на все эти мероприятия, ртуть все же теряется в виде шлама вместе с продуктами осмоления. Ее расход составляет 1-1,5 кг на 1 т ацетальдегида.[4, с. 195]
В промышленности процесс проводят при температуре 75-100 °С, пропуская ацетилен через водный катализаторный раствор. При 50 % конверсии ацетилена выход альдегида составляет 92-93% от прореагировавшего ацетилена. Основную реакцию осуществляют в полой футерованной колонне, заполненной катализаторным раствором и имеющей расширение в верхней части (заполненной насадкой).[3, с. 442]
Большим недостатком процесса синтеза ацетальдегида по Кучерову является необходимость применения дорогостоящей и весьма токсичной металлической ртути и ее соединений. Металлическая ртуть летуча; несмотря на высокую температуру кипения (357°С), она испаряется уже при комнатной температуре. При повышенной температуре в условиях процесса гидратации ртуть проникает почти во все аппараты установки и в получаемые продукты. Следствием этого являются значительные потери ртути и возможность профессиональных заболеваний у обслуживающего персонала.[5, с. 489]
Вместе с тем этот способ обладает многими преимуществами, которые могут быть успешно реализованы в других технологиях. В частности, этот процесс является одностадийным, обладает хорошей селективностью, может обеспечить одновременное получение двух целевых продуктов (ацетальдегид и кротоновый альдегид). Кроме того, реактор обеспечивает не только проведение собственно реакции, но и отделение продуктов от катализаторного раствора. Эффективное применение рециркуляции как по воде, так и ацетилену обеспечивает не только полное использование сырья, но и служит для подавления побочных реакций, повышая выход целевого продукта. Все это делает процесс достаточно привлекательным, однако высокотоксичная каталитическая система делает его бесперспективным.[3, с. 446]
Смотрите также
Выводы
В
результате проделанной работы решена задача разделения промышленной смеси
продуктов синтеза хлорбензола. В качестве модели наиболее адекватно описывающей
парожидкостное равновесие смеси была выбр ...
Молекулы. Химическая связь. Строение веществ
Химические частицы, образованные из двух или
нескольких атомов, называются молекулами (реальными или условными
формульными единицами многоатомных веществ). Атомы в молекулах химически
связаны.
П ...
Особенности сорбционного извлечения палладия (II) из хлоридных растворов волокнами ЦМ-А2, Мтилон-Т и ВАГ
Одним из
перспективных направлений в комплексном решении экологических проблем является
разработка высокоэффективных процессов очистки промышленных газовоздушных
выбросов, сточных вод и сре ...


