Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Мольный изобарно-изотермический потенциал реакции полиме-
ризацииУчим химию / Определение термодинамических параметров реакции полимеризации тетрафторэтилена / Учим химию / Определение термодинамических параметров реакции полимеризации тетрафторэтилена / Мольный изобарно-изотермический потенциал реакции полиме-
ризации Мольный изобарно-изотермический потенциал реакции полиме-
ризацииСтраница 2
По полученным данным построим графики зависимости термодинамических величин от температуры (рис. 1-4).
Исходя из расчетов, можно сделать вывод о том, что с ростом температуры, энтальпия реакции полимеризации стремится в положительную область, а это означает уменьшение теплового эффекта при увеличении температуры проведения процесса. Так же видно, то, что энтропия системы отрицательна, и с возрастанием температуры стремится к нулевому значению. Увеличение абсолютного значения энергии Гиббса также можно определить из графика. В виду того, что энергия Гиббса не на всем интервале температур принимает отрицательные значения, протекание реакции термодинамически вероятно лишь в интервале Т ≈ 340 К.
Из графика зависимости константы равновесия от температуры можно сделать вывод о том, что целесообразно проводить реакцию при низких температурах, поскольку при температуре 270 К константа равновесия принимает наибольшее значение, что говорит о сильном смещении равновесия в сторону образования продукта реакции (полимера).

Рис. 1. Зависимость энтальпии реакции от температуры
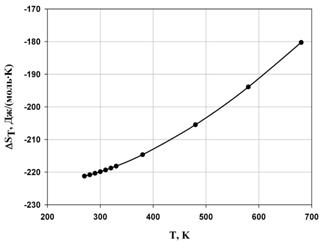
Рис. 2. Температурная зависимость энтропии реакции
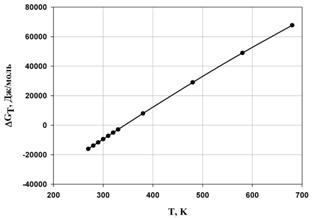
Рис. 3. Зависимость энергии Гиббса от температуры.
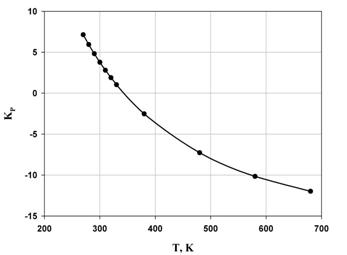
Рис. 4. Температурная зависимость константы равновесия.
3.
Рассчитаем предельную температуру проведения полимеризации тетрафторэтилена:
Тпр = 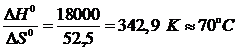
4.
Проведем расчет реакционных способностей для случая сополимеризации тетрафторэтилена и этилена:
Эти мономеры имеют следующие значения реакционной способности и полярности (константы Алфрея – Прайса):
е Q
Тетрафторэтилен 1,22 0,0049
Этилен -0,20 0,015
Тогда:
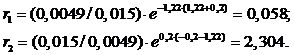
Получим, что ![]() . Это свидетельствует о том, что сополимеризация не является статистической.
. Это свидетельствует о том, что сополимеризация не является статистической.
В сополимере присутствует больше этилена, чем тетрафторэтилена, поскольку ![]() .
.
Рассчитаем состав сополимера:
Пусть f1 – доля тетрафторэтилена, f2 – этилена в смеси мономеров. Зададим: f1 = 0,1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8; 0,9 и, соответственно, f2 = 0,9; 0,8; 0,7; 0,6; 0,5; 0,4; 0,3; 0,2; 0,1.
Тогда пользуясь уравнением для расчета состава полимера:
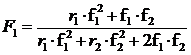 ,
,
рассчитаем состав сополимера.
Результаты расчетов представлены в таблице:
|
f 1 |
f 2 |
F1 |
F2 |
|
0,1 |
0,9 |
0,027 |
0,973 |
|
0,2 |
0,8 |
0,030 |
0,970 |
|
0,3 |
0,7 |
0,034 |
0,966 |
|
0,4 |
0,6 |
0,039 |
0,961 |
|
0,5 |
0,5 |
0,047 |
0,953 |
|
0,6 |
0,4 |
0,059 |
0,941 |
|
0,7 |
0,3 |
0,079 |
0,921 |
|
0,8 |
0,2 |
0,120 |
0,880 |
|
0,9 |
0,1 |
0,238 |
0,762 |
Смотрите также
Биокерамика на основе фосфатов кальция
В последние годы значительное
внимание уделяется созданию керамических материалов медицинского назначения, предназначенных
для использования при реконструкции дефектов костных тканей, образу ...
Физико-химические основы хроматографического процесса
Газовая хроматография — один из
наиболее перспективных физико-химических методов исследования, бурно
развивающийся в настоящее время. Создание и успешная разработка различных
вариантов газо ...
Фотоколориметрическое определение салициловой кислоты в фармпрепаратах
...


