Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Молекулярная масса и структураУчим химию / Обзор и математическое моделирование суспензионной полимеризации тетрафторэтилена / Учим химию / Обзор и математическое моделирование суспензионной полимеризации тетрафторэтилена / Молекулярная масса и структура Молекулярная масса и структураСтраница 1
Молекулярная масса ПТФЭ впервые была определена с помощью меченой серы (35S), введенной в полимер при инициировании полимеризации окислительно-восстановительной системой Fe3+ + Na2SO3. Косвенно молекулярная масса М может быть определена по теплоте кристаллизации, поскольку скорость кристаллизации из расплава и степень кристалличности охлажденных образцов зависит от М. Наиболее широко применяемый метод оценки М ПТФЭ основан на зависимости плотности спеченных образцов от М, вытекающей из указанной выше связи степени кристалличности и М, и различия в плотностях кристаллических и аморфных областей (рис. II. 6). Для этого метода требуется учитывать пористость образца. Истинная плотность может быть определена по ИК-спектру (по полосе поглощения 12,8 мкм). Плотность кристаллического ПТФЭ при 23°С, найденная экстраполяцией зависимости плотности от степени кристалличности, равна 2,304 ± 0,006 г/м3. Рентгеноструктурный анализ дает результаты ниже, чем ИК-спектроскопия, на 5 и на 10% при степени кристалличности 90 и 50% соответственно. Для промышленных образцов ПТФЭ ![]() = 4·105 - 107. ПТФЭ с
= 4·105 - 107. ПТФЭ с ![]() =106 и более может быть получен только при использовании ТФЭ высокой степени чистоты. Глубокая очистка ТФЭ, который, как правило, производится на том же заводе, что и ПТФЭ, необходима для синтеза полимера не только с высокой молекулярной массой, но и не содержащего в основной цепи никаких других атомов кроме С и F.
=106 и более может быть получен только при использовании ТФЭ высокой степени чистоты. Глубокая очистка ТФЭ, который, как правило, производится на том же заводе, что и ПТФЭ, необходима для синтеза полимера не только с высокой молекулярной массой, но и не содержащего в основной цепи никаких других атомов кроме С и F.
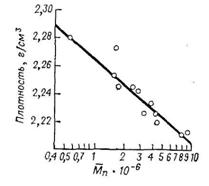
Рис. 2. Зависимость плотности ПТФЭ от молекулярной массы
Введение в цепь таких атомов, как Н и Сl, снижает термостойкость полимера. Наличие, например, атомов водорода в полимерной цепи при 370—390 °С (при температуре переработки) приводит к отщеплению HF и последующему разрыву цепи, снижающему М полимера и ухудшающему свойства готовых изделий. Поэтому присутствие в ТФЭ незначительных количеств таких примесей, как трифторэтилен, которые легко сополимеризуются с ТФЭ, может влиять на качество изделий.
Расчетным путем можно оценить, что при содержании водородсодержащих непредельных примесей менее 10-5 % свойства ПТФЭ практически сохраняются; а в присутствии 10-4 % примесей и больше возможно существенное ухудшение качества полимера. Предельные фторорганические соединения, содержащие водород или хлор, как было показано в предыдущих разделах, могут обрывать цепи. Допустимые количества конкретных соединений должны устанавливаться экспериментально.
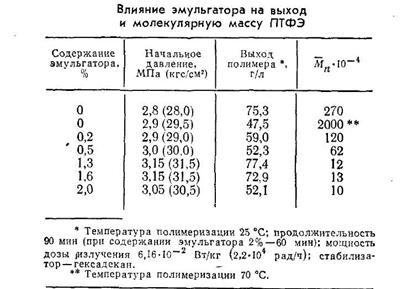
Молекулярная масса эмульсионного ПТФЭ несколько ниже, чем суспензионного, и достигает 2,5·106 — 3,5·106. Это связано с более высокой температурой полимеризации, другой, по сравнению с суспензионной полимеризацией, инициирующей системой, коллоидной формой частиц полимера, поверхность которых смачивается водой за счет сорбции ПАВ, и наличием стабилизатора (углеводорода), способного участвовать в реакциях передачи цепи. При эмульсионной полимеризации под действием γ-облучения, как уже отмечалось, продукты радиолиза перфторэмульгатора снижают М . Зависимость ![]() от концентрации C7F15COONH4 и условий полимеризации, приведены в (табл. 2).
от концентрации C7F15COONH4 и условий полимеризации, приведены в (табл. 2).
Таблица 2
Степень кристалличности ПТФЭ непосредственно после полимеризации высокая (93—98%). Температура плавления такого полимера 342 °С (на 15 °С выше температуры плавления образцов, хоть раз подвергшихся спеканию) [53, с. 630]. При повторном спекании температура плавления ПТФЭ уже не меняется.
Степень кристалличности спеченного ПТФЭ колеблется от 50 до 70% и зависит как от молекулярной массы, так и от скорости охлаждения образцов. При быстром охлаждении (закалке) получаются образцы с минимальной степенью кристалличности. Для эмульсионного ПТФЭ степень кристалличности спеченных образцов может достигать 70—85%. Максимальная скорость кристаллизации наблюдается при 310—315 0С.
Молекула ПТФЭ в кристаллическом состоянии имеет форму спирали (рис. II. 7). Такую форму молекула принимает в связи с тем, что атомы фтора имеют большой ван-дер-ваальсов радиус и при плоской зигзагообразной конформации, как у полиэтилена, не укладываются на длине 0,254 нм (2,54 Å), соответствующей расстоянию между двумя атомами углерода, разделенными третьим атомом. Поворот каждой связи С—С от плоского расположения примерно на 17° увеличивает это расстояние до 0,27 нм (2,7 Å), что близко к удвоенному ван-дер-ваальсову радиусу фтора 0,28 нм (2,8 Å). Угол между связями С—С составляет 116°.


