Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Химические свойства альдегидов и кетонов. Присоединение кислородных нуклеофиловУчим химию / Учим химию / Химические свойства альдегидов и кетонов. Присоединение кислородных нуклеофилов Химические свойства альдегидов и кетонов. Присоединение кислородных нуклеофиловСтраница 2
1-этоксиэтанол
(полуацеталь)
Полуацетали обычно не выделяют из реакционной смеси из-за их неустойчивости. Исключение составляют циклические полуацетали, образующиеся самопроизвольно из g - и d-гидроксиальдегидов. Например, доля циклического полуацеталя в его равновесной смеси с 5-гидроксипентаналем составляет 94%.
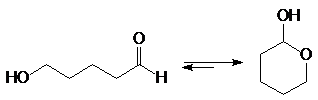 (34)
(34)
5-оксипентаналь
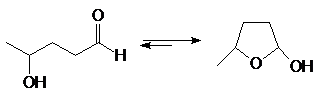 (35)
(35)
4-оксипентаналь
Полуацетали при взаимодействии со второй молекулой спирта в присутствии сильных кислот и при условии удаления воды в результате реакции нуклеофильного замещения могут превращаться в полные ацетали.
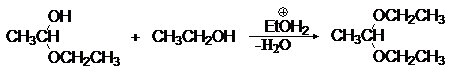 (36)
(36)
1,1-диэтоксиэтан
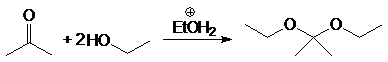 (37)
(37)
Механизм образования ацеталей и кеталей на первом этапе AN, а на втором SN1.
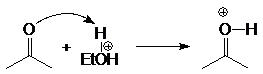
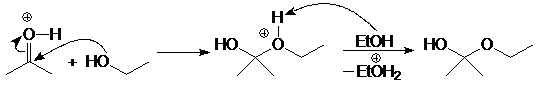 (м 6)
(м 6)
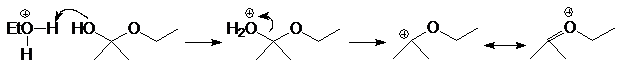
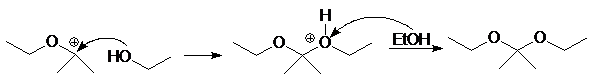
Вместо двух молекул спирта можно использовать одну молекулу диола:
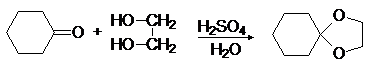 (38)
(38)
этилендиоксициклогексан
Ацетали обладают структурой простых эфиров и подобно простым эфирам устойчивы к щелочам и нуклеофильным реагентам, но гидролизуются водными кислотами, причем гораздо легче, чем простые эфиры: уже при комнатной температуре под действие разбавленных минеральных кислот:
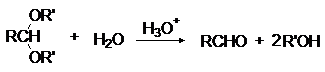
Устойчивость ацеталей и кеталей к действию нуклеофильных реагентов позволяет защищать карбонильную группу при проведении реакции по другим группам с нуклеофильными реагентами. После чего карбонильную группу рекуперируют. Для такой защиты чаще всего используют этиленгликоль:
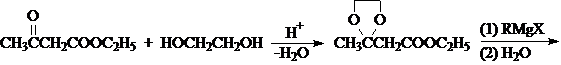
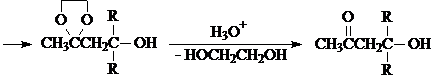
Присоединение серосодержащих нуклеофилов.
Атом серы тиолов является лучшим нуклеофилов, чем атом кислорода спиртов. Тиолы реагируют с карбонильными соединениями в кислой среде, образуя дитиоацетали.
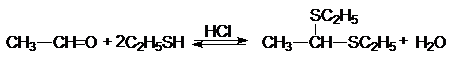 (39)
(39)
1,1-ди(этилтио) этан (дитиоацеталь)
С этилендитио-1,2-диолом и 1,3-пропандитиолом образуются циклические тиоацетали.
При нагревании тиокеталей с никелем Ренея в спирте происходит десульфурирование, в результате чего исходная карбонильная группа превращается в метиленовую и таким образом достигается восстановление альдегидов и кетонов в углеводороды.
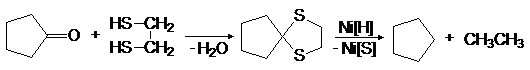 (40)
(40)
циклический тиокеталь
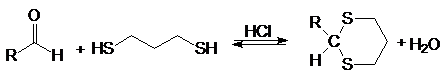 (41)
(41)
1,3-пропандитиол 1,3-дитиан
(циклический тиоацеталь)
Дитиоацетали обладают СН-кислотными свойствами (pKa 31), поэтому при действии сильных оснований, например, литийорганических соединений, они отщепляют протон, образуя карбанион, отрицательный заряд которого делокализуется при участии 3d-орбиталей атома серы. В результате происходит обращение полярности реакционного центра (Umpolung): карбонильный атом углерода (электрофильный центр) превращается в карбанион, обладающий нуклеофильными свойствами.
Смотрите также
Произврдство в доменой печи и сплавы
...
Дмитрий Иванович Менделеев
...
Пептиды и первичная структура белка
Пептиды и белки
представляют собой высокомолекулярные органические соединения, построенные из
остатков α-аминокислот, соединенных между собой пептидными связями.
Ни один из
известны ...


