Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ЭнтропияСтраница 1
Наиболее информативной термодинамической функцией в уравнении (19) является энтропия S.
Значение энтропии легко определить только для состояния идеального газа. Используем для вычисления S уравнение (18), где dU — изменение внутренней энергии, равное для идеального газа СvdT т.е. теплоемкости при постоянном объеме, умноженной на приращение температуры: pdv — приращение работы, которое можно представить как![]() , заменив р на RT/v. Отсюда
Лучшие проститутки тулы ждут вашего звонка. | Шлюхи Наро-Фоминска гарантируют конфиденциальность и безопасность.
, заменив р на RT/v. Отсюда
Лучшие проститутки тулы ждут вашего звонка. | Шлюхи Наро-Фоминска гарантируют конфиденциальность и безопасность.
![]() (20)
(20)
После интегрирования в пределах 0¾T получаем
![]() (21)
(21)
|
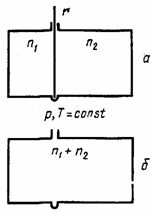
рис. 2 Схема для расчета энтропии при самопроизвольном смешивании двух газов. |
где ST — энтропия при температуре Т; S0 — энтропийная постоянная; Сv — теплоемкость при постоянном объеме; v — молярный объем. Таким образом, энтропия моля идеального газа является функцией Т и р (так как молярный объем зависит от Т и р). Выражение (21) применимо лишь для чистого идеального газа, так как для смесей газов, даже при отсутствии между ними химических реакций, энтропия смеси будет возрастать за счет необратимых процессов диффузии, приводящей к распределению компонентов по всему объему газовой смеси. Рассмотрим процесс самопроизвольного смешения двух газов. Пусть в двух частях объема, разделенного перегородкой r (рис. 2, а), находится n1 молей первого газа и n2 молей второго газа при р, Т=const. |
Общая энтропия системы
![]() (22)
(22)
где S1 и S2 — молярные энтропии первого и второго газов. Удалим перегородку r и дадим возможность газам образовать смесь, равномерно распределенную по всему объему ![]() (рис 2,б), где v —молярный объем газа при данных р и Т. На каждый моль компонентов смеси приходятся пропорциональные части объема:
(рис 2,б), где v —молярный объем газа при данных р и Т. На каждый моль компонентов смеси приходятся пропорциональные части объема:
![]() и
и ![]()
Подставляем значения этих объемов в уравнение (21) и получаем значения энтропии для одного моля компонента в смеси:
![]()
![]()
Общий запас энтропии в смеси газов тоже увеличился:
![]() (23)
(23)
Приращение энтропии в газовой смеси зависит от соотношения чисел молей компонентов n1 и n2. Если положить, что n1 → 0, то энтропия этого газа
![]()
но доля, вносимая этим компонентом в общий запас энтропии системы, также стремится к нулю: ![]() . В то же время если n1→ 0, то (n1+n2)/n2 стремится к 1, а
. В то же время если n1→ 0, то (n1+n2)/n2 стремится к 1, а ![]() тоже стремится к нулю. Следовательно, при исчезновении одного из компонентов газовой смеси энтропия другого компонента станет равна энтропии чистого газа:
тоже стремится к нулю. Следовательно, при исчезновении одного из компонентов газовой смеси энтропия другого компонента станет равна энтропии чистого газа:
Смотрите также
Выбор конструкционного материала
аппарата и опор
Оборудование
современных процессов нефтепереработки и нефтехимии должно работать при низких
и высоких температурах, значительных механических напряжениях, в агрессивных
рабочих средах. Поэтому мате ...
Ядерная химия
Наряду со стабильными изотопами
данного химического элемента известны многочисленные изотопы химических
элементов, способные самопроизвольно превращаться в изотопы других химических
элементов посре ...
Технология приготовления косметических гелей
На
фоне довольно высоких темпов развития химической промышленности сегодня
ученому-исследователю очень трудно уследить за тенденциями развития
производства косметической продукции еще и по ...