Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Расчет изменения энтропии реакцииУчим химию / Физическая химия / Учим химию / Физическая химия / Расчет изменения энтропии реакции Расчет изменения энтропии реакции
Изменение Энтропии системы в результате протекания процесса определяется по уравнению:
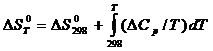 (6)
(6)
В этом уравнении ∆S0298 – стандартное изменение энтропии для реакции при 298 К, определяемое по мольным энтропиям веществ ∆S0i,298:
![]() (7)
(7)
Значение ∆S0298 для соответствующих веществ приведены в табл. 1, после их подстановки в уравнение (7) получим:
∆S0298 = ∆S0298(н2о) + ∆S0298(cos) – (∆S0298(н2s) + ∆S0298(co2)) =
= 231,53 + 188,72 - (213,66+205,70) = 0,89 Дж/К
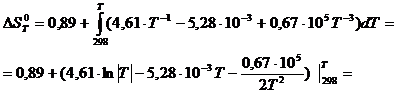
= 0,89 +(4,61∙ln│Т│- 5,28∙10-3∙Т – 0,335∙105∙Т-2) – (26,3 – 1,57 – 0,38)=
= 4,61∙ln│Т│- 5,28∙10-3∙Т – 0,335∙105∙Т-2 – 23,46
Рассчитаем изменение энтропии в заданном интервале температур и полученные данные сведем в табл. 3.
∆S0800 = 4,61∙ln│800│- 5,28∙10-3∙800 – 0,335∙105∙800-2 – 23,46 = 3,079 Дж/К
…………………………………………………………………………………
∆S01700 =4,61∙ln│1700│–5,28∙10-3∙1700–0,335∙105∙1700-2 – 23,46 = 1,843 Дж/К
Таблица 3.
Значения изменения энтропии (∆S0т ) при различных Т,К
|
Т, К |
800 |
900 |
1000 |
1100 |
1200 |
1300 |
1400 |
1500 |
1600 |
1700 |
|
∆S0т, Дж |
3,08 |
3,11 |
3,07 |
2,99 |
2,87 |
2,71 |
2,53 |
2,32 |
2,09 |
1,84 |
По данным табл. 3 построим график ∆S0т = f(Т) (см. рис. 2).
Смотрите также
Исследование совместного электровосстановления гадолиния и
алюминия в галогенидных расплавах.
Из анализа
литературных данных следует, что процесс электровосстановления алюминия из
хлоридных и фторидных расплавов изучался в основном на платиновом электродах.
Электровосстановление
алюминия ...
Характеристика сим–триазиновых пестицидов и их содержание в различных объектах окружающей среды
Возделываемые культуры обладают разной конкурентной способностью к сорнякам в борьбе за свет, влагу и питательные элементы. Чем больше экологические требования сорняков совпадают с требованиями ку ...
Значение химии в создании новых материалов, красителей и волокон
...


