Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Индукционные взаимодействия Ван-дер-Ваальса (эффект Дебая)Учим химию / Физическая связь / Учим химию / Физическая связь / Индукционные взаимодействия Ван-дер-Ваальса (эффект Дебая) Индукционные взаимодействия Ван-дер-Ваальса (эффект Дебая)
Молекула, обладающая постоянным дипольным моментом, наводит в другой молекуле, неполярной или полярной, так называемый индуцированный дипольный момент. Величина индуцированного электрическим полем напряженности E
дипольного момента mинд
может быть представлена следующим рядом: mинд =
a
E+
b
E2+
¼
. Для электрических полей малой напряженности можно пренебречь всеми членами ряда, кроме первого, это приближение можно сделать для пары индукционно взаимодействующих диполей. mинд =
a
E
, где a - поляризуемость молекулы. Индуцированный дипольный момент имеет то же направление, что и линии напряженности электрического поля постоянного диполя вызвавшего появление наведенного дипольного момента у поляризуемой молекулы или радикала в точке нахождения поляризуемой молекулы (или соответственно радикала). Взаимодействие постоянного диполя одной молекулы (радикала, сложного иона) и наведенного им диполя второй молекулы (или вообще группы атомов) понижает потенциальную энергию системы из двух молекул и упрочняет систему.
Пусть в неполярной молекуле, отстоящей от полярной молекулы на расстоянии s, индуцируется момент mинд. Энергия Uинд взаимодействия молекул зависит от напряженности E поля, создаваемого в центре неполярной частицы постоянным дипольным моментом полярной молекулы и от величины индуцированного момента mинд: 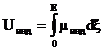
. Интеграл берется от 0 до E, так как изначально поля в центре неполярной молекулы нет, и, возникая под внешним влиянием полярной молекулы, оно растет от 0 до E. Подставив в выражение для Uинд ранее полученное выражение для μинд, получим: Uинд=‑
½
a
E
2
. Напряженность E поля создаваемого в центре неполярной молекулы положительным и отрицательным полюсами постоянного диполя может быть выражена следующей формулой:
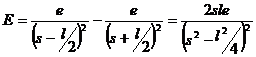 .
.
Здесь, как и раньше, пренебрегая l2 по сравнению с s2, получим: ![]() . Подставив полученное для напряженности выражение в формулу энергии индукционного взаимодействия (Uинд=‑½aE2) получаем: Uинд=‑
. Подставив полученное для напряженности выражение в формулу энергии индукционного взаимодействия (Uинд=‑½aE2) получаем: Uинд=‑
2
a
m
2
/
s
6
.
Если учесть, что наводящая индуцированный дипольный момент молекула сама обладает поляризуемостью, формула примет окончательный вид:
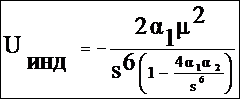
Энергия индукционного взаимодействия, как и ориентационного, убывает пропорционально шестой степени расстояния, но индукционное взаимодействие не зависит от температуры. Последнее связано с тем, что ориентация наведенного дипольного момента не может быть произвольной, она однозначно определяется направлением и положением наводящего диполя в пространстве.
Величина энергии индукционного взаимодействия Uинд тем значительнее, чем выше поляризуемость поляризуемых молекул. Индукционное взаимодействие наблюдается: при образовании гидратов благородных газов, в растворах полярных веществ, в неполярных растворителях (например, ацетона в тэтрахлорметане) и т.п., но существенно только для молекул со значительной поляризуемостью; к ним, в первую очередь, относятся молекулы с сопряженными связями.
Индукционное взаимодействие не аддитивно. Это становится ясным, если рассмотреть неполярную частицу в поле двух симметрично расположенных диполей. Каждый из них, действуя сам, вызвал бы индукционный эффект, но совместное их действие взаимно уравновешивается, в результате чего дипольный момент у неполярной частицы не наводится, а следовательно энергия системы в рассматриваемом случае индукционным взаимодействием не понижается.
В следствие нераспространенности легко поляризуемых молекул и неаддитивности индукционных взаимодействий эффект Дебая никогда не бывает доминирующим по сравнению с эффектом Кезома (ориентационные взаимодействия) и с эффектом Лондона (см. ниже).
Смотрите также
Анализ технической серной кислоты и олеума
Раствор триоксида
серы в серной кислоте называется олеумом. Его широко применяют в
промышленности, например для очистки нефтепродуктов, изготовления некоторых
красителей, производства взрыв ...
Жесткость
Вода, в которой
растворены соли кальция и магния, обладает особым свойством – жесткостью.
Жесткость, обусловленная содержанием гидрокарбонатов кальция и магния,
называется карбонатной. Ее находят т ...


