Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Реакции ацилирования органостаннанов.Библиотека / Реакции a-литиированных циклических нитронов с электрофильными реагентами / Библиотека / Реакции a-литиированных циклических нитронов с электрофильными реагентами / Реакции ацилирования органостаннанов. Реакции ацилирования органостаннанов.
В 1942 году советскими химиками было показано, что алкил- и арилстаннаны реагируют с ацилирующими агентами в присутствии AlCl3.[lvi]
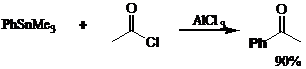
Взаимодействие хлорангидридов кислот с органостаннанами в присутствии нуклеофильных катализаторов Et4N+Br- и Et4N+Cl- позволило авторам провести реакцию в отсутствии хлорида алюминия. При этом выход кетона 89
составил 100 процентов.
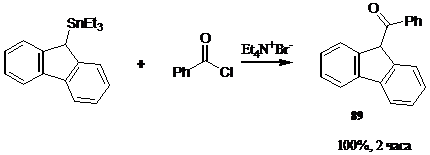
Хлорангидриды кислот реагируют с органостаннанами в условиях реакции Стилле с образованием кетонов. Реакция не осложняется образованием третичных спиртов, что зачастую наблюдается при взаимодействии литий- и магнийорганических соединений с хлорангидридами кислот.41
Хлорангириды ароматических, алифатических и гетероциклических кислот могут быть введены в реакцию Стилле; выходы данной реакции составляют от 75 до 100%, а время проведения реакции не превышает одного часа.
Таким образом, например, были получены кетоны ацетиленового ряда.[lvii]
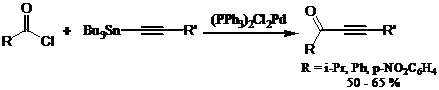
Взаимодействие триалкилпиридилстаннанов с хлорангидридами кислот открыло новый перспективный способ получения производных пиридина, многие из которых являются биологически активными соединениями.[lviii]
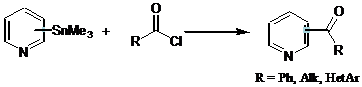
Интересно отметить, что взаимодействие 2-триметилстаннилпиридина с бензоилхлоридом при комнатной температуре происходит за 3 часа с выходом 70% даже без участия катализатора, в то время как 3- и 4-замещённые производные пиридина реагирует только в присутствии катализатора за 10 часов.
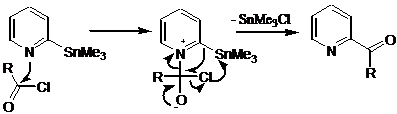
Авторы предлагают возможную интерпретацию данного неожиданно лёгкого ацилирования во второе положение пиридинового цикла: реакция начинается с нуклеофильной атаки атома азота пиридинового цикла на карбонильную группу хлорангидрида кислоты с образованием четвертичной соли с последующей миграцией ацильной группы к a-атому углерода с образованием продукта реакции.
Реакция образования кетонов активно используется в синтезе природных соединений. Так, ключевой интермедиат в синтезе антибиотика пуренофорина был получен по реакции Стилле, причём реакция происходит с сохранением Z-конфигурации реагирующего a,b-ненасыщенного сложного эфира.[lix]
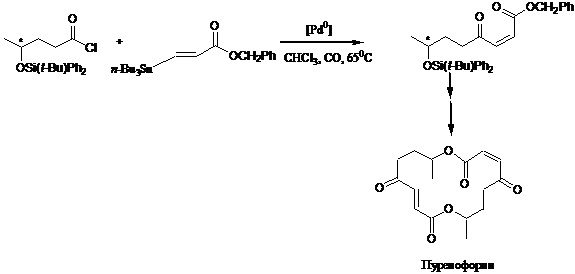
Симметричные 1,2-дикетоны могут быть получены из хлорангидридов ароматических кислот. Реакция проводится с ½ эквивалента Et6Sn2, взаимодействие которого с хлорангидридом бензойной кислоты 91приводит к образованию оловоорганического реагента 92
, взаимодействие которого в свою очередь с хлорангидридом кислоты 91
приводит к образованию продукта реакции 93
.

Смотрите также
Легко- и трудногидролизуемые полисахариды
Определение легко - и трудногидролизуемых
полисахаридов в древесине основано на реакциях их гидролиза с последующим
нахождением общего количества образовавшихся моносахаридов по редуцирующей ...
Алкалоиды и история их открытия
...
Характеристика сим–триазиновых пестицидов и их содержание в различных объектах окружающей среды
Возделываемые культуры обладают разной конкурентной способностью к сорнякам в борьбе за свет, влагу и питательные элементы. Чем больше экологические требования сорняков совпадают с требованиями ку ...


