Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Относительная стабильность карбанионов.
Пространственное строение карбанионовОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Относительная стабильность карбанионов.
Пространственное строение карбанионов Относительная стабильность карбанионов.
Пространственное строение карбанионовСтраница 1
Для простых алкильных карбанионов, например, СН3-, можно предположить пирамидальную sp3-гибридизованную или плоскую sp2-гибридизованную конфигурацию:
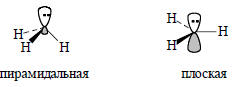
В первом случае орбиталь, несущая отрицательный заряд, является sp3-гибридной орбиталью, а во втором - чистой р-орбиталью. Электронной паре выгоднее находиться на sp3-орбитали, чем на р-орбитали, поскольку sp3-орбиталь имеет на 25% характер s-орбитали, а s-орбиталь ближе к ядру и имеет более низкую энергию, чем р-орбиталь (гл. 1). По этой причине простые алкильные карбанионы должны иметь пирамидальную конфигурацию. Другая причина предпочтительности пирамидальной конфигурации состоит в том, что в ней репульсивное взаимодействие (отталкивание) между неподеленной парой и тремя электронными парами связей С-Н значительно меньше, чем в плоской конфигурации. https://facedigital.agency топ 30 smm агентств.
Под влияние тепла пирамидальные алкильные анионы все время находятся в процессе инверсии пирамидальной структуры. Рассчитанный барьер инверсии для СН3- составляет около 5 ккал/моль:
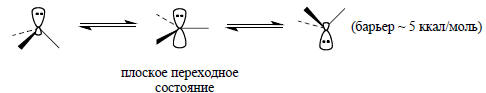
При понижении температуры скорость инверсии пирамиды уменьшается. Например, в реакции оптически активного 2-октиллития с СО2 при -70оС образуется смесь карбоновых кислот с суммарным сохранением конфигурации на 20% (т.е. 60% молекул реагирует с сохранением, а 40% - с обращением конфигурации), однако при 0оС продукт полностью рацемизован. Это согласуется со схемой реакции, в которой ковалентное (см. гл. 19) литийорганическое соединение диссоциирует до карбанионов, которые вследствие быстрой инверсии переходят в равновесную смесь энантиомерных пирамидальных структур. При -70оС атака молекулой СО2 происходит еще до полного установления равновесия, а при 0оС равновесие успевает установиться перед атакой:
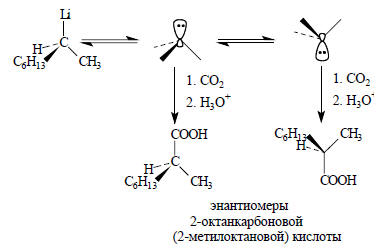
Скорость инверсии пирамидальной конфигурации сильно зависит от структуры карбаниона. Если карбанионный центр входит в состав трехчленного цикла, то барьер инверсии значительно повышается. В молекуле циклопропана имеется значительное напряжение, так как углы между связями равны 60о вместо 109,5о в нормальном тетраэдре. В ходе процесса инверсии напряжение еще более увеличивается, поскольку в плоской геометрии карбаниона угол между связями кольца должен возрасти до 120о, а он остается равным 60о. Вследствие этого цис-2-метилциклопропиллитий при действии СО2 дает исключительно (т.е. стереоспецифично) цис-2-метилциклопропанкарбоновую кислоту:
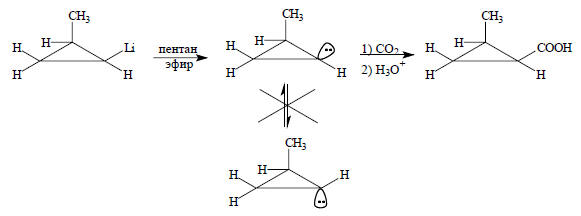
Изотопный обмен водорода в 1-циано-2,2-дифенилциклопропане по этой же причине протекает с сохранением конфигурации:
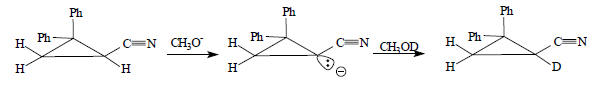
Таким образом, можно сделать вывод, что для алкильных карбанионов характерна пирамидальная конфигурация. В связи с этим следует отметить, что карбанионы изоэлектронны аминам, а, как известно, амины существуют в виде быстро взаимопревращающихся друг в друга пирамидальных форм:
Смотрите также
Анализ технологического процесса схемы переэтерификации диметилового эфира цианоэтилфосфоновой кислоты моноэтиленгликоль (мет) акрилатом
История развития
человечества - это прежде всего история изобретения, создания и
совершенствования различных изделий и технологий, другими словами - процесса
инженерного творчества (ИТ). Ре ...
Методы получения наночастиц
Изучение
наноструктур интенсивно началось примерно двадцать лет назад, и уже занимает
определенное место в сфере применения. Хотя слово нанотехнология является
относительно новым, устройств ...
Амилолитические ферменты и их применение в спиртовой промышленности
...


