Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Жесткие и мягкие кислоты и основанияОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Жесткие и мягкие кислоты и основания Жесткие и мягкие кислоты и основанияСтраница 2
Принцип ЖМКО формулируется следующим образом: жесткие основания Льюиса предпочитают координироваться с жесткими кислотами; мягкие основания - с мягкими кислотами.
Деление кислот и оснований на мягкие и жесткие не является ни абсолютным, ни резко разграниченным. Поскольку жесткость и мягкость являются сравнительными качествами, существуют классы кислот и оснований, имеющие пограничные свойства. Некоторые мягкие основания обладают высоким сродством к протону (жесткой кислоте); примером является ион S2-, который, однако, осаждается ионами меди и серебра (мягкие кислоты), но не осаждается ионами железа и алюминия (жесткие кислоты). Мягкие кислоты не обязательно образуют более стабильные аддукты с более тяжелыми (более мягкими) элементами V-VIII групп, хотя жесткие кислоты всегда предпочитают кооординироваться с более легким элементом. Однако в целом жесткость основания увеличивается в группе Периодической системы снизу вверх, например:
I-<Br-<Cl-<F-
В изоэлектронных сериях оснований жесткость возрастает в периоде слева направо:
NH2-<OH-<F-
Жесткость кислот в группах периодической таблицы возрастает снизу вверх, например:
Li+>Na+>K+
Zn2+>Cd2+>Hg2+
Классификация кислот и оснований по жесткости и мягкости дается в табл. 3.1
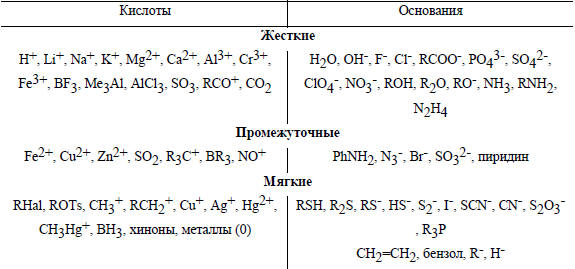
Таблица 3.1
Качественное деление на жесткие, промежуточные и мягкие кислоты и основания
Смотрите также
Химические элементы, их связи и валентность
Мир химии
существует миллиарды лет. Химические явления сопровождают всю нашу жизнь и даже
определяют саму возможность ее существования.
Вторая половина
XX века ознаменовала новый виток р ...
Катионы второй аналитической группы
...
Развитие алхимии
...


